
【题目】聚苹果酸(PMLA)可作为目的合成药物的载体,它的一种化学合成路线如下:
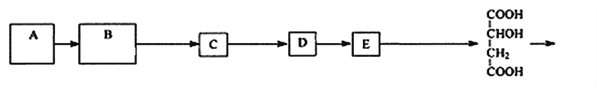
己知:琼斯试剂能选择性氧化含不饱和碳的醇,而醇中的碳碳双键或三键不受影响:RCH=CHCH2OH![]() RCH=CHCOOH
RCH=CHCOOH
回答下列问题:
(1)A的结构简式是_______________, D生成E的反应类型是______________。
(2)D中官能团的名称是______________________。在浓硫酸和加热条件下,1mol苹果酸最多能与_______mol碳酸氢钠反应。
(3)写出B → C的化学方程式:________________________________________。
(4)化合物F是B与氢气的加成产物,F的同分异构体共有_________种(不含立体异构,不包括F)。
(5)參照上述合成路线,以异戊二烯[CH2=C(CH3)CH=CH2]为原料(无机试剂任选)设计制备![]() 的合成路线:______________________。
的合成路线:______________________。
【答案】 CH2=CH—CH=CH2 加成反应 羧基、碳碳双键 2 Cl-CH2CH=CHCH2-Cl + 2H2O![]() HO-CH2CH=CHCH2-OH+2HCl或Cl-CH2CH=CHCH2-Cl + 2NaOH
HO-CH2CH=CHCH2-OH+2HCl或Cl-CH2CH=CHCH2-Cl + 2NaOH![]() HO-CH2CH=CHCH2-OH+2NaCl 8
HO-CH2CH=CHCH2-OH+2NaCl 8 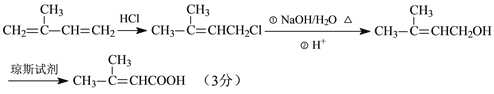
【解析】根据有机物HOOC-CH(OH)-CH2-COOH倒推可知,E为HOOC-CH(Cl)-CH2-COOH, D为HOOC-CH=CH-COOH, C在琼斯试剂作用下,氧化为D,C为HOCH2-CH=CH-CH2OH, B为ClCH2-CH=CH-CH2Cl, A为CH2=CH-CH=CH2。
(1)由以上分析可知A的结构简式是CH2=CH—CH=CH2 ; D为HOOC-CH=CH-COOH, E为HOOC-CH(Cl)-CH2-COOH,所以D与氯化氢发生加成反应生成E;正确答案:CH2=CH—CH=CH2 、加成反应。
(2)有机物D为HOOC-CH=CH-COOH, D中官能团的名称是羧基、碳碳双键;只有羧基与碳酸氢钠溶液反应,且1摩尔羧基与1摩尔碳酸氢钠溶液反应;在浓硫酸和加热条件下,1mol苹果酸最多能与2mol碳酸氢钠反应;正确答案:羧基、碳碳双键 ; 2 。
3)有机物B为ClCH2-CH=CH-CH2Cl,有机物C为HOCH2-CH=CH-CH2OH,所以B → C在氢氧化钠溶液中加热反应即可实现,B → C的化学方程式:Cl-CH2CH=CHCH2-Cl + 2H2O![]() HO-CH2CH=CHCH2-OH+2HCl;正确答案:Cl-CH2CH=CHCH2-Cl + 2H2O
HO-CH2CH=CHCH2-OH+2HCl;正确答案:Cl-CH2CH=CHCH2-Cl + 2H2O![]() HO-CH2CH=CHCH2-OH+2HCl或Cl-CH2CH=CHCH2-Cl + 2NaOH
HO-CH2CH=CHCH2-OH+2HCl或Cl-CH2CH=CHCH2-Cl + 2NaOH![]() HO-CH2CH=CHCH2-OH+2NaCl。
HO-CH2CH=CHCH2-OH+2NaCl。
(4)B为ClCH2-CH=CH-CH2Cl,与氢气的加成产物ClCH2-CH2-CH2-CH2Cl, 化合物F的可能结构为:四个碳的饱和烃有2种结构,分别为正丁烷和异丁烷,然后分别进行正丁烷上发生二元取代有6种,异丁烷上发生二元取代有3种,如果除去括F,还有8种;正确答案8。
(5)CH2=C(CH3)CH=CH2与氯化氢发生1,2加成反应生成含有一个双键的氯代烃,再在氢氧化钠的水溶液作用下加热反应生成含有双键的醇,根据题给信息RCH=CHCH2OH![]() RCH=CHCOOH 可知,含有双键的醇被琼斯试剂氧化为羧酸;整个流程如下:
RCH=CHCOOH 可知,含有双键的醇被琼斯试剂氧化为羧酸;整个流程如下: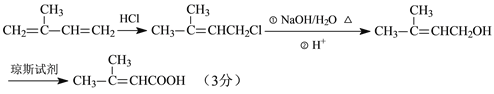 ;正确答案:
;正确答案: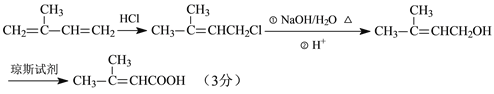 。
。


科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)甲基的电子式_________________。
(2)写出4-甲基-2-乙基-1-戊烯的键线式___________________________。
(3)有机物![]() 系统名称是_______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是___________________。
系统名称是_______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是___________________。
(4)①等物质的量的A.甲醇、B.乙醇、C.乙二醇、D.丙三醇,分别和足量的金属钠作用,放出氢气的量由少到多的顺序是_______________;
②等质量的A.甲醇、B.乙醇、C.乙二醇、D.丙三醇,分别和足量的金属钠作用,放出氢气的量由少到多的顺序是_______________。
提示:甲醇:CH3OH、乙二醇:![]() 、丙三醇:
、丙三醇:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验描述、对应的现象以及结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A | 向滴有酚酞的Na2CO3溶液中加入BaCl2固体 | 溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
B | 处理锅炉水垢中的CaSO4 时,依 次加入饱和Na2CO3溶液和盐酸 | 水垢溶解 | Ksp:CaCO3>CaSO4 |
C | 其它条件不变,平衡体系: FeCl3(aq)+3KSCN(aq) +3KCl(aq)中,加KCl 固体 | 红色变浅 | 证明增大生成物KCl的浓度,使原溶液中化学平衡逆向移动 |
D | 向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 先出现 黄色沉淀 | Ksp:AgCl<AgI |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A. ![]() <1.0×10-7mol/L
<1.0×10-7mol/L
B. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-)
D. c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法错误的是()
A. 常温常压下,4gD2O中含有的电子数为2NA
B. 42gC2H4和C4H8的混合气中含有氢原子数为6NA
C. 25℃时,pH=1的H3PO4溶液中含有H+数为0.1NA
D. H2O(g)通过Na2O2(s)使其增重bg时,反应中转移的电子数为bNA/2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列溶液中微粒浓度关系一定正确的是
A. 0.1molLNa2CO3溶液,加水稀释,c(HCO3-)/c(CO32-)减小
B. pH=7的氨水与氯化氨的混合溶液中:c(Cl-)>c(NH4+)
C. 0.1molL的硫酸铝溶液中:c(SO42-)>c(Al3+)>c(H+)>c(OH-)
D. pH=2的醋酸溶液和pH=12的NaOH溶液等体积混合:c(Na+)=c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是生物体细胞内部分有机化合物的概念图,请回答下列问题。

(1)小麦种子中的储能物质c是________,人和动物细胞中的储能物质c是________。
(2)组成b的多肽是由氨基酸通过脱水缩合连接而成,脱水缩合是指____________________。
(3)用洋葱鳞片叶______(填“内”或“外”)表细胞,可以通过染色来观察DNA和e的分布,实验操作步骤中要用盐酸水解,目的有改变细胞膜的通透性,加速染色剂进入细胞,同时使______________________,利于DNA与染色剂结合。
(4)人体摄入的d中_______参与血液中脂质的运输,维生素D能有效地促进__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于平衡常数的说法正确的是( )
A. 在平衡常数表达式中,反应物浓度用起始浓度,生成物浓度用平衡浓度
B. 在任何条件下,化学平衡常数是一个恒定值
C. 平衡常数的大小与温度、浓度、压强、催化剂等无关
D. 从平衡常数的大小可以推断一个反应进行的程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com