
【题目】下列关于动植物糖类、脂质的叙述中,正确的是
A. 核糖、葡萄糖、脱氧核糖是动植物体内共有的单糖
B. 葡萄糖、果糖、蔗糖均为还原性糖
C. 只有多糖、蛋白质、脂肪三类生物大分子以碳链为骨架
D. 固醇包括了脂肪、性激素、维生素D
科目:高中化学 来源: 题型:
【题目】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料.
(1)在25℃、101kPa时,16gCH4完全燃烧生成液态水时放出的热量是890.31kJ,则CH4燃烧的热化学方程式为_____________,
(2)已知:C(s)+O2(g)═CO2(g);△H=﹣437.3 kJmol﹣1
H2(g)+O2(g)═H2O(g);△H=﹣285.8 kJmol﹣1
CO(g)+O2(g)═CO2(g);△H=﹣283.0 kJmol﹣1
则煤气化反应C(s)+H2O(g)═CO(g)+H2(g) 的焓变△H=__________kJmol﹣1;
(3)如图所示组成闭合回路,其中,甲装置中CH4为负极,O2和CO2的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出,CuSO4溶液的体积为200mL.

①装置中气体A为___________(填“CH4”或“O2和CO2”),d极上的电极反应式为___________;
②乙装置中a极上的电极反应式为_________.若在a极产生112mL(标准状况)气体,则甲装置中消耗CH4______mL(标准状况),乙装置中所得溶液的pH=_________.(忽略电解前后溶液体秋变化)
③如果乙中电极不变,将溶液换成饱和Na2SO3溶液,当阴极上有a mol气体生成时,同时有w g Na2SO410H2O晶体析出,若温度不变,剩余溶液中溶质的质量分数应为______________(用含w、a的表达式表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种物质间的转化关系如图所示,下列转化关系中不能一步实现的是 ( )
选项 | X | Y | Z | W |
A | Na | Na2O2 | NaOH | NaCl |
B | H2S | SO2 | SO3 | H2SO4 |
C | Fe | FeCl3 | Fe(OH)3 | Fe2O3 |
D | AlCl3 | NaAlO2 | Al(OH)3 | Al |

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,下列各组离子在指定溶液中一定能大量共存的是
A. pH=1的无色溶液中:Na+、Cu2+、Cl-、![]()
B. 使酚酞呈红色的溶液中:K+、Na+、NO3-、Cl-
C. 0.1 mol·L-1的FeCl2溶液中:H+、Al3+、SO42-、S2-
D. 由水电离出的c(H+)=1×10-10 mol·L-1的溶液中:Mg2+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:
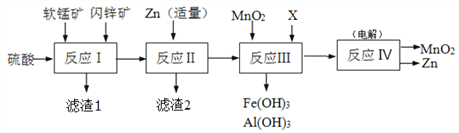
已知:反应Ⅰ中所有金属元素均以离子形式存在。
回答下列问题:
(1)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应的离子方程式________________________________。
(2)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,滤渣2的主要成分是______(填名称)。
(3)反应Ⅲ中MnO2的作用是______,另外一种物质X可以是______。(填字母代号)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反应Ⅳ中电极均是惰性电极,写出阳极电极反应式_______________。本工艺可以循环利用的物质有MnO2、Zn和_____。
(5)已知:H2S的电离常数K1=1.0×107,K2=7.0×1015。0.1 mol/L NaHS的pH___7(填“>”“=”或“<”),理由是________________________________________。
(6)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L1 Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS浓度为1.0×104 mol·L1时,Mn2+开始沉淀,则a=________。[已知:Ksp(MnS)=1.4×1015]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 天然气的主要成分是甲烷,它属于不可再生能源
B. 煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料
C. 石油分馏得到的汽油、煤油、柴油等都有混合物,没有固定的熔沸点
D. 石油炼制的目的是为了获得轻质油和重要化工原料(乙烯、丙烯等)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中进行的反应:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) △H 。在某压强下起始时按不同氢碳比[n(H2)/n(CO2)]投料(见右图中曲线①②③),测得CO2的平衡转化率与温度关系如下图所示,
C2H5OH(g)+3H2O(g) △H 。在某压强下起始时按不同氢碳比[n(H2)/n(CO2)]投料(见右图中曲线①②③),测得CO2的平衡转化率与温度关系如下图所示,

下列有关说法正确的是
A.该反应:△H >0
B.氢碳比:①<②<③
C.其它条件不变的情况下,缩小容器的体积可提高CO2的转化率
D.若起始CO2浓度为2mol·L-1、H2为4mol·L-1,在图中曲线③氢碳比条件下进行,则400K时该反应的平衡常数数值约为1.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量转换的说法正确的是( )
A. 煤燃烧是化学能全部转化为热能的过程
B. 化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C. 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D. 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14g乙烯和丙烯混合气体中的氢原子数为2NA
B. 27g铝中加入1mol/L的NaOH溶液,转移电子数是3NA
C. 1 molFe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,44. 8LNO与22. 4LO2反应后的分子数是2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com