
【题目】2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2=2CO2 +3H2O,电池示意图如下,下列说法中正确的是
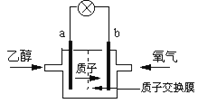
A.b极为电池的负极
B.电池工作时电子在内电路中由a极经溶液到b极
C.电池负极的电极反应为:C2H5OH+3H2O-12e-=2CO2+12H+
D.电池工作时,1mol乙醇被氧化时有6mol电子转移
【答案】C
【解析】
试题分析:A.在燃料电池中,燃料乙醇在负极发生失电子的反应,氧气是在正极上发生得电子的反应,则a为负极,故A错误;B.电池工作时,电子在外电路中由a极经溶液到b极,内电路中是电解质溶液中的阴阳离子定向移动,故B错误;C.在燃料电池中,正极上是氧气得电子的还原反应,在酸性电解质环境下,正极的电极反应为:4H++O2+4e-=2H2O,燃料乙醇在负极发生失电子的氧化反应,负极的电极反应为:C2H5OH+3H2O-12e-=2CO2+12H+,故C正确;D.根据电池反应:C2H5OH+3O2=2CO2+3H2O,则1mol乙醇被氧化失去12mol电子,所以1mol乙醇被氧化电路中转移12NA的电子,故D错误;答案为C。


科目:高中化学 来源: 题型:
【题目】A,B,C,D,E,F为6种短周期主族元素,它们的核电荷数依次递增,已知:B原子核外最外层电子数是次外层电子数的两倍,电子总数是E原子电子总数的 ![]() ,F是同周期元素中原子半径最小的元素:D2﹣与E2+的电子层结构相同.B与D可以形成三原子化合物甲;A是非金属元素,且A,C,F可形成离子化合物乙.请回答:
,F是同周期元素中原子半径最小的元素:D2﹣与E2+的电子层结构相同.B与D可以形成三原子化合物甲;A是非金属元素,且A,C,F可形成离子化合物乙.请回答:
(1)F元素的名称是 , E的元素符号是 .
(2)写出化合物乙的电子式 .
(3)化合物甲有个σ键,个π键.
(4)B,C,D三种元素组成的气态氢化物的稳定性由强到弱的顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2气体分别通入下列四种溶液中,有关现象及结论的说法正确的是( ) 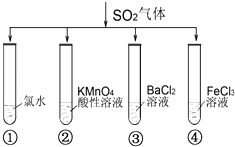
A.试管①中有淡黄色沉淀生成,说明SO2有氧化性
B.试管②中溶液褪色,说明SO2有漂白性
C.试管③中能产生白色沉淀,说明SO2有酸性
D.试管④中溶液颜色变浅,说明SO2有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D均是短周期元素,A和B同周期,B和C同族,A元素族序数是周期数的三倍,B原子最外层电子数是内层电子数的二倍,B与A能生成化合物BA2 , C与A生成化合物CA2 , A的阴离子与D的阳离子电子层结构相同,都与氖原子的电子层结构相同,D 的单质与A 的单质在不同条件下反应,可生成D2A或D2A2 . 请回答
(1)写出元素符号B:C:
(2)BA2的电子式 , BA2分子中化学键属于键..
(3)D2A2的化学式 , 灼烧这化合物火焰呈色.
(4)C在元素周期表中的位置是第周期,族,其原子结构示意图 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+ . AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+ . 若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是(填序号).
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是(填序号).
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI﹣淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,请写出反应的离子方式: .
(4)Fe与过量稀硫酸反应可以制取FeSO4 . 若用反应所得的酸性溶液,将Fe2+转化为Fe3+ , 要
求产物纯净,可选用的最佳试剂是(填序号).
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2:1,试配平下列方程式:
FeSO4+K2O2→ K2FeO4+K2O+K2SO4+O2↑
当转移了1.5NA个电子时,在标况下可收集到 L氧气.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com