
【题目】现有一种有机物M,其结构简式为![]() ,M的同分异构体有多种,符合下列条件的同分异构体有( )
,M的同分异构体有多种,符合下列条件的同分异构体有( )
①六元环上有3个取代基,②官能团不变,③两个基团不连接在同一个碳原子上。
A. 9种B. 10种C. 11种D. 12种
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组为了验证元素非金属性递变规律,设计了如图所示的两套实验方案进行实验探究:
(1)根据方案一装置![]() 如图
如图![]() 回答以下问题:
回答以下问题:
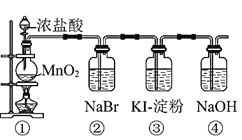
Ⅰ![]() 写出装置①中发生反应的化学方程式:______。
写出装置①中发生反应的化学方程式:______。
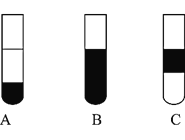
Ⅱ![]() 若将反应后②中的溶液倒入
若将反应后②中的溶液倒入![]() 中,出现的现象与图中吻合的是______。
中,出现的现象与图中吻合的是______。![]() 填代号
填代号![]()
Ⅲ![]() 装置③中的现象是______。
装置③中的现象是______。
(2)根据方案二装置![]() 如图
如图![]() 回答以下问题:
回答以下问题:

Ⅰ![]() 方案二验证元素非金属性递变的理论依据是:______。
方案二验证元素非金属性递变的理论依据是:______。
Ⅱ![]() 装置的作用是______,X是______。
装置的作用是______,X是______。
Ⅲ![]() 能说明碳元素与硅元素非金属性强弱的实验现象是______。
能说明碳元素与硅元素非金属性强弱的实验现象是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,科学家已经研制出世界上最薄的材料——碳膜片,其厚度只有一根头发的二十万分之一。如图所示,这种碳膜片形状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
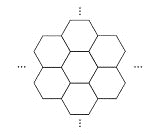
A. 碳膜片属于一种新型的化合物
B. 碳膜片与石墨的结构相同
C. 碳膜片与C60互为同素异形体
D. 碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法中合理的是( )

A. 可以选用方案1分离碳酸氢钠中含有的氯化铵
B. 方案1中的残留物应该具有的性质是受热易挥发
C. 方案2中加入的试剂一定能够与除X外的物质发生化学反应
D. 方案2中加入NaOH溶液可以分离出SiO2和Fe2O3混合物中的Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态K原子中,核外电子占据最高能层的符号是____,占据该能层电子的电子云轮廓图形状为______。
(2)基态Ge原子的核外电子排布式为[Ar]_______,有______个未成对电子。
(3)写出基态As原子的核外电子排布式____。根据元素周期律,原子半径Ga___As,第一电离能Ga____As。(填“大于”或“小于”)
(4)Zn2+基态核外电子排布式为____________________。
(5)氮原子价层电子的轨道表达式(电子排布图)为_____________。
(6)CH4和CO2所含的三种元素电负性从小到大的顺序为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的发明是化学对人类的一项重大贡献。
I:如图所示,烧杯中都盛有稀硫酸。
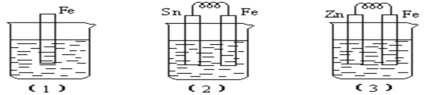
(1)中反应的离子方程式为______________,
(2)中的电极反应:Fe:______________、Sn:______________Sn极附近溶液的pH______________(填增大、减小或不变),
(3)中被腐蚀的金属是______________、比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是______________
II:依据氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+ 设计的原电池如图所示。
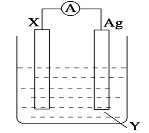
(1)电极 X 的材料是_____;电解质溶液 Y 是_____。
(2)Ag 电极上发生的反应为:_________。
(3)针对上述原电池装置,下列说法中不正确的是_____。(双选)
A.原电池工作时的总反应:Cu+2Fe3+=2Fe2++Cu2+
B.原电池工作时,X 电极流出电子,发生氧化反应
C.原电池工作时,银电极上发生氧化反应
D.原电池工作时,阴离子向 Ag 极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时生成的水的质量和消耗氧气的质量不变的是
A. CH4O,C3H4O5B. C3H6,C3H8O
C. C3H8,C4H6D. C2H6,C4H6O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物结构或性质的描述,不正确的是
A. C4H9OH发生催化氧化反应,可生成3种有机产物
B. 光照下,Cl2可在甲苯的苯环上发生取代反应
C. 异戊二烯可发生加聚反应,生成高分子化合物
D. 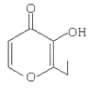 的分子式为C7H8O3
的分子式为C7H8O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、锌和100 mL稀硫酸反应,小组同学根据实验过程绘制的标准状况下的气体体积V与时间 t的图像如下图所示。
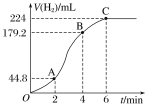
①在OA、AB、BC三段中反应速率最快的是_________,原因是__________________________。
②2~4 min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)为________________。
③为了减缓反应速率而又不改变产生氢气的量,该同学在硫酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.0.5mol/L盐酸
其中,你认为可行的是(填序号)______________.
Ⅱ、在一个小烧杯里加入约20 g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10 g氯化铵晶体,并立即用玻璃棒迅速搅拌。试回答下列问题:
(1)实验中要立即用玻璃棒迅速搅拌的原因是______________________________。
(2)“结冰”现象说明该反应断开旧化学键________(填“吸收”或“放出”)的能量________(填“>”或“<”)形成新化学键________(填“吸收”或“放出”)的能量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com