
【题目】氮元素有多种氧化物。请回答下列问题:
(1)已知:H2的燃烧热ΔH为-285.8kJ·mol-1。
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(1) ΔH=-44kJ·mol-1
则4H2(g) + 2NO2(g) = 4H2O(g) + N2(g) ΔH=__________。
(2)一定温度下,向2L恒容密闭容器中充入0.40mol N2O4,发生反应:N2O4(g)![]() 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
c(NO2)/(mol·L-1) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
①0-40s内,v(NO2)=________mol·L-1·s-1。
②升高温度时,气体颜色加深,则上述反应是________(填“放热”或“吸热”)反应。
③该温度下反应的化学平衡常数K=________mol·L-1。
④相同温度下,若开始向该容器中充入0.80molN2O4,则达到平衡后c(NO2)________ (填“>”“=”或“<”)0.60mol·L-1。
(3)N2O5是绿色硝化试剂,溶于水可得硝酸。下图是以N2O4为原料电解制备N2O5的装置。写出阳极区生成N2O5的电极反应式(注意阳极区为无水环境,HNO3亦无法电离):________________________。

(4)湿法吸收工业尾气中的NO2,常选用烧碱溶液,产物为两种常见的含氧酸盐。该反应的离子方程式是____________________。
【答案】4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=-1100.2kJ·mol-1 0.005 吸热 1.8 < N2O4-2e-+2HNO3=2N2O5+2H+ 2NO2 + 2OH— = NO2— + NO3— + H2O
【解析】
(1)①H2(g)+1/2O2(g)═H2O(l);△H=-285.8kJ·mol-1,
②N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
③H2O(g)=H2O(1) ΔH=-44kJ·mol-1
由盖斯定律①×4-②-③×4得:4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=-1100.2kJ·mol-1;
(2)①由速率公式计算。②根据平衡移动原理判断;③根据平衡常数表达式计算;④建立与原平衡放大2倍的等效平衡,然后将体积缩小到与原平衡相同。
(3)阳极发生氧化反应,注意非水体系,硝酸写化学式;
(4)湿法吸收工业尾气中的NO2,常选用烧碱溶液,产物为两种常见的含氧酸盐,硝酸盐和亚硝酸盐。写出反应方程式。
(1)①H2(g)+1/2O2(g)═H2O(l);△H=-285.8kJ·mol-1,
②N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
③H2O(g)=H2O(1) ΔH=-44kJ·mol-1
由盖斯定律①×4-②-③×4得:4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=-285.8KJ·mol-1×4-133kJ·mol-1+44kJ·mol-1×4=-1100.2kJ·mol-1;
(2) N2O4(g)![]() 2NO2(g)
2NO2(g)
c始(mol·L-1) 0.2 0
c变(mol·L-1) 0.15 0.3
c平(mol·L-1 ) 0.05 0.3
①0-40s内,v(NO2)=0.2mol·L-1÷40s=0.005mol·L-1·s-1。
②升高温度时,气体颜色加深,平衡正向移动,则上述反应是吸热反应。
③该温度下反应的化学平衡常数K=![]() =1.8mol·L-1。
=1.8mol·L-1。
④相同温度下,若开始向该容器中充入0.80molN2O4,相当于将原平衡放大2倍,然后加压,平衡逆向移动,则达到平衡后c(NO2)<0.60mol·L-1。
(3)以N2O4为原料电解制备N2O5,N2O4失电子被氧化,阳极区生成N2O5的电极反应式为:N2O4-2e-+2HNO3=2N2O5+2H+。
(4)湿法吸收工业尾气中的NO2,常选用烧碱溶液,产物为两种常见的含氧酸盐,硝酸盐和亚硝酸盐,该反应的离子方程式是2NO2 + 2OH— = NO2— + NO3— + H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某实验小组学生用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算反应热.下列说法正确的是 ( )

A. 如图条件下实验过程中没有热量损失
B. 图中实验装置缺少环形玻璃搅拌棒
C. 烧杯间填满碎纸条的作用是固定小烧杯
D. 若改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L的NaOH溶液进行反应,从理论上说所求反应热相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂不仅是营养物质和主要食物,也是一种重要的工业原料。下面是以油脂为主要原料获得部分产品的合成路线:

己知:①G (C10H10O4)分子中的官能团处于对位;
②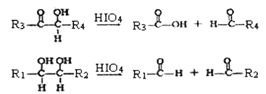
(R1、R2、R3与R4可能是氢、烃基或其他基团)
回答下列问题:
(1)下列关于油脂的说法正确的是____。(填标号)
a.油脂包括植物油和脂肪,属于酯类
b.天然油脂是混合甘油酯组成的混合物,无固定的熔点和沸点
c.油脂属天然高分子化合物,许多油脂兼有烯烃的化学性质
d.硬化油又叫人造脂肪,便于储存和运输,但容易被空气氧化变质
(2)G中官能团的名称为______,反应①的反应类型为_________。
(3)用系统命名法写出F的名称___________。
(4)在酸催化下物质的量的B与苯酚反应生成一种线型结构高分子的化学方程式为______________________。
(5)二元取代芳香化合物H是G的同分异构体,H满足下列条件:
①能发生银镜反应
②酸性条件下水解产物物质的量之比为2:1
③不与NaHCO3溶液反应。
则符合上述条件的H共有______种(不考虑立体结构,不包含G本身)。其中核磁共振氢谱为五组峰的结构简式为________(写出一种即可)。
(6)写出从HOCH2CH2OH![]() HCOOCH2CH2OOCH的合成路线(无机试剂任选,合成路线参照题中的书写形式)______________。
HCOOCH2CH2OOCH的合成路线(无机试剂任选,合成路线参照题中的书写形式)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. CaCO3溶于CH3COOH溶液中:CaCO3+2H+=Ca2++CO2↑+H2O
B. 向AlCl3溶液中通入过量NH3:Al3++4OH—=![]() +2H2O
+2H2O
C. 过量的铁和稀硝酸反应:Fe+![]() +4H+=Fe3++NO↑+2H2O
+4H+=Fe3++NO↑+2H2O
D. 向KAl(SO4)2溶液中滴入Ba(OH)2溶液使![]() 恰好完全沉淀:
恰好完全沉淀:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于有机物![]() 的叙述正确的是
的叙述正确的是
A. 在一定条件下1mol该物质最多与4molH2发生加成反应
B. 该物质不能与碳酸氢钠反应放出二氧化碳
C. lmol该物质与足量的金属钠反应生成2molH2
D. 该物质含羟基与苯环直接相连的结构且能水解的同分异构体有19种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物甲有镇咳、镇静的功效,其合成路线如下:
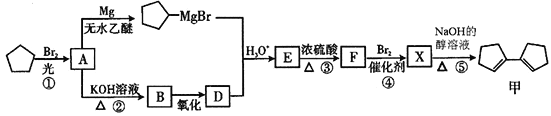
已知: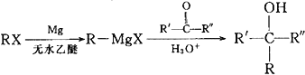 (R、R'、R"代表烃基或氢)
(R、R'、R"代表烃基或氢)
(1)有机物甲的分子式为___________,有机物A中含有的官能团的名称为_______________。
(2)有机物B的名称是__________,由B→D 所需的反应试剂和反应条件为________________。
(3)在上述①~⑤反应中,属于取代反应的有____________(填序号)。
(4)写出E→F的化学方程式________________。
(5)满足“属于芳香族化合物”的甲的同分异构体有________种。其中核磁共振氢谱上只有2组峰的结构简式是______________
(6)根据题给信息,写出以CH4为原料制备CH3CHO的合成路线(其他试剂任选)__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种关于酸的使用,其中正确的是
A. 为了抑制Fe2+的水解,用稀硝酸酸化 B. 检验溶液中是否含有SO![]() 时,先用盐酸酸化
时,先用盐酸酸化
C. 乙酸与乙醇的酯化反应中,浓硫酸起到了催化剂和脱水剂的作用 D. 为了增强KMnO4溶液的氧化能力,用浓盐酸酸化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C、D、E、F为周期表中前四周期的七种元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同。
请回答下列问题:
(1)D元素的原子中存在________种运动状态的电子;
(2)在A元素与上述其他元素形成的分子中,其中心原子为sp3杂化的为________(写出2种即可)
(3)与C同族且位于第四周期元素所形成简单气态氢化物的电子式为________;其与C的简单气态氢化物相比稳定性更________(填“强”或“弱”);
(4)F的基态原子核外电子排布式是_____________________________;其在元素周期表中的位置是:_______________________________;
(5)E原子的第一电离能比同周期后面相邻元素的第一电离能________(填“大”或“小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用下列各组物质序号填空:
① O2和O3 ; ② 12C、13C、14C; ③ C2H6和C5H12; ④C3H6和C5H10;⑤14N、14C
⑥ ![]() 和
和![]() ;⑦ CH3 (CH2) 3 CH3和
;⑦ CH3 (CH2) 3 CH3和![]()
互为同位素的是______; 互为同素异形体的是_______ ; 互为同系物的是_______;互为同分异构体的是_______ ;属于同一物质的是 _______ 。
(2)除去溴苯中的溴:试剂是:________,反应的化学方程式为____________________
(3)一定质量的乙醇在氧气不足时燃烧,得到CO、CO2和H20质量共为27.6g,若H2O的质量为10.8g,则CO2的质量为_____________g
(4)2g C2H2完全燃烧生成液态水和CO2,放出99.6kJ热量,则C2H2燃烧热的热化学方程式:_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com