
依据元素周期表及元素周期律,下列推断正确的是
A.H3BO3的酸性比H2CO3的强 B.氢氧化钡的碱性比氢氧化钙的碱性强
C.硒化氢比硫化氢稳定 D.若Xm+ 和Yn- 核外电子层结构相同,则在周期表中X、Y的族序数之差一定为:(m+n)-8
科目:高中化学 来源: 题型:
在阿司匹林的结构简式(如图)中①②③④⑤⑥分别标出了
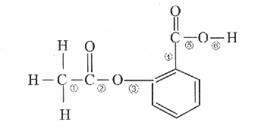 其分子不同的键。将阿司匹林与足量NaOH溶液共热时,发生反应时断键的位置是( )
其分子不同的键。将阿司匹林与足量NaOH溶液共热时,发生反应时断键的位置是( )
A.①④
B.②⑤
C.③④
D.②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作的说法正确的是
A.可用25ml碱式滴定管量取20.00 ml KMnO4 溶液
B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C.用量筒量取5.00 mL 1. 00mol·L-1盐酸于50mL容量瓶中,加水稀释至刻度可配
制0.100mol·L-1盐酸
D.中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH <0 的化学反应下列叙述不正确的是
A.该反应是放热反应 B.ΔH的值与反应方程式的计量系数有关
C.若将该反应设计成原电池则锌为负极
D.若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
熔融盐燃料电池具有高的发电效率,因而受到重视。用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,可制得在650℃下工作的燃料电池。已知该电池总反应为:2CO+O2=2CO2。则下列说法中正确的是( )
A.通CO的一极是电池的正极,
B.该电池工作过程中需不断补充CO和O2,CO2可循环利用
C.负极反应式:O2+2CO2+4e-==2CO32-
D.该电池工作过程中有蓝色火焰产生
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强。

(1) 写出X在周期表中的位置 。
(2)W的简单离子的还原性比Y简单离子的还原性 (填强或弱);Z的气态氢化物和溴化氢相比,较稳定的是 (写化学式)。
(3)Y与W形成的化合物和Z单质水溶液反应,生成二种强酸,该反应的化学方程式是 。
(4)已知25℃时,2.3gC2H5OH(l)在足量的W单质充分反应后恢复原状,放出68.34kJ热量, 则该反应的热化学方程式:
 (5)已知N2(g)+2O2(g)===2 NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=—534 kJ·mol-1,根据盖斯定律写出肼( N2H4)与NO2完全反应生成氮气和气态水的热化学方程式________________。
(5)已知N2(g)+2O2(g)===2 NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=—534 kJ·mol-1,根据盖斯定律写出肼( N2H4)与NO2完全反应生成氮气和气态水的热化学方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
快乐是什么?精神病学专家通过实验发现:在大脑的相应部位——“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺结构如图,下列说法错误的是 ( )
A.多巴胺分子式为C8H11NO2。
B.多巴胺可以发生加成、取代、氧化反应。
C.和溴水反应时,1 mol多巴胺可以消耗6 mol溴单质。
D.多巴胺既可与强酸反应,又可以与强碱反应。

查看答案和解析>>
科目:高中化学 来源: 题型:
运用元素周期律分析下面的推断,其中错误的是( )
A.硒化氢是无色、有毒、比硫化氢稳定的气体
B.砹化银不溶于水也不溶于稀硝酸
C.硫酸镭是难溶于水的白色固体
D.锗单质是一种优良的半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com