
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强。

(1) 写出X在周期表中的位置 。
(2)W的简单离子的还原性比Y简单离子的还原性 (填强或弱);Z的气态氢化物和溴化氢相比,较稳定的是 (写化学式)。
(3)Y与W形成的化合物和Z单质水溶液反应,生成二种强酸,该反应的化学方程式是 。
(4)已知25℃时,2.3gC2H5OH(l)在足量的W单质充分反应后恢复原状,放出68.34kJ热量, 则该反应的热化学方程式:
 (5)已知N2(g)+2O2(g)===2 NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=—534 kJ·mol-1,根据盖斯定律写出肼( N2H4)与NO2完全反应生成氮气和气态水的热化学方程式________________。
(5)已知N2(g)+2O2(g)===2 NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=—534 kJ·mol-1,根据盖斯定律写出肼( N2H4)与NO2完全反应生成氮气和气态水的热化学方程式________________。
科目:高中化学 来源: 题型:
下列实验操作与预期实验目的或实验结论不一致的是
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 在0.1 mol·L-1的NaHCO3溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深 | 验证盐类水解反应是吸热反应 |
| C | 将一定量的NaNO3和KCl的混合液加热并 浓缩至有晶体析出时,趁热过滤 | 得到NaCl晶体 |
| D | 苯酚钠溶液中通入足量二氧化碳产生浑浊 | 苯酚的酸性弱于碳酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
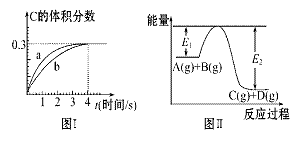
将1 mol A(g)和2 mol B(g)置于2 L某密闭容器中,在一定温度下发生反应:
A(g)+B(g) C(g)+D(g),并达到平衡。C的体积分数随时间变化如图Ⅰ中曲线b
C(g)+D(g),并达到平衡。C的体积分数随时间变化如图Ⅰ中曲线b
所示,反应过程中的能量变化如图Ⅱ所示,下列说法不正确的是( )
A.反应在第4秒钟达到化学平衡状态,0~4秒内,以A表示的化学反应速率是:0.225 mol·L-1·s-1
B.该温度下,反应的平衡常数数值约为7.36
C.恒温条件下,缩小反应容器体积可以使反应的过程按图Ⅰ中a曲线进行
D.在上述反应体系中加入催化剂,化学反应速率增大,E1和E2均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期表及元素周期律,下列推断正确的是
A.H3BO3的酸性比H2CO3的强 B.氢氧化钡的碱性比氢氧化钙的碱性强
C.硒化氢比硫化氢稳定 D.若Xm+ 和Yn- 核外电子层结构相同,则在周期表中X、Y的族序数之差一定为:(m+n)-8
查看答案和解析>>
科目:高中化学 来源: 题型:
已知铅蓄电池Pb + PbO2 + 2H2SO4 ==2PbSO4 + 2H2O 在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。下列说法中正确的是
A.标有“+”的接线柱,充电时作阳极,放电时作负极
B.放电时PbO2作正极,电池工作一段时间后电解质溶液密度会减少
C.充电时电路中通过0.1mol电子时,电解质溶液有0.2molH2SO4 产生
D.充电时阳极中PbSO4 被还原为PbO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
A.SO2和SiO2 B.CCl4和KCl C.NaCl和HCl D.CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.在多电子的原子里,能量高的电子通常在离核近的区域内运动
B.最外层电子数为8的微粒均是稀有气体元素的原子
C.俄国化学家道尔顿为元素周期表的建立作出了巨大贡献
D.在周期表中金属和非金属的分界线附近寻找制备半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,体积为2 L的密闭容器中,NO2和N2O4之间发生反应:
2NO2 (g) (红棕色)
 N2O4(g) (无色),如图所示。
N2O4(g) (无色),如图所示。
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若升高温度,则v(正) ,v(逆) 。
(填“加快”或“减慢”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=18 mol/(L·min),乙中v(N2O4)=0.2 mol/(L·s),则 中反应更快。
(4)在0到1 min中内用X表示该反应的速率是 ,该反应达限度时,Y的转化率 ,反应开始时与反应达平衡状态时的压强之比为 。
(5)若反应达平衡状态时再升高温度,容器内混合气体颜色加深,则正反应是 反应。
(填“放热”或“吸热”。已知:降低温度有利于放热反应)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com