
| m |
| M |
| 13g |
| 65g/mol |


科目:高中化学 来源: 题型:
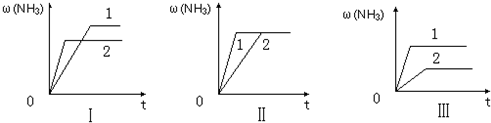
查看答案和解析>>
科目:高中化学 来源: 题型:
 蛋白质在腐败时,常会产生氨气,写出氨气的电子式
蛋白质在腐败时,常会产生氨气,写出氨气的电子式查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是制取无水氯化铜(易潮解)的实验装置图,A中装有MnO2,从B中滴入浓盐酸,E为石英玻璃管,内装细铜粉,F中装有碱石灰(生石灰和氢氧化钠)固体.请回答下列问题:
如图是制取无水氯化铜(易潮解)的实验装置图,A中装有MnO2,从B中滴入浓盐酸,E为石英玻璃管,内装细铜粉,F中装有碱石灰(生石灰和氢氧化钠)固体.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 为探究NH3的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题:
为探究NH3的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.3g金属钠变成钠离子时失去的电子数目为0.2NA |
| B、通常状况下,22.4L氢气中所含分子数目为NA |
| C、1molNH3中所含的电子数为10NA |
| D、1 mol/L的NaCl溶液中含NA个钠离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、构成单质分子的微粒中不一定含有化学键 |
| B、只含有共价键的物质一定是共价化合物 |
| C、NaCl溶于水破坏了离子键,乙醇溶于水破坏了共价键 |
| D、CaCl2 中既有共价键又有离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com