
| A. | ${\;}_{\;}^{13}$O和14O互称同素异形体 | B. | 丙烷和异丁烷互称同系物 | ||
| C. | 金刚石和石墨互称同位素 | D. | 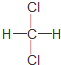 和 和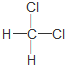 互称同分异构体 互称同分异构体 |
分析 A、同种元素形成的不同种单质互成同素异形体;
B、结构相似、在分子组成上相差一个或若干个CH2原子团的化合物互成同系物;
C、同种元素的不同种原子间互成同位素;
D、分子式相同而结构不同的化合物互成同分异构体.
解答 解:A、同种元素形成的不同种单质互成同素异形体,而13O和14O是两种原子而不是单质,故不是同素异形体,故A错误;
B、丙烷和异丁烷的结构相似、是在分子组成上相差一个CH2原子团的化合物,故互成同系物,故B正确;
C、同种元素的不同种原子间互成同位素,而金刚石和石墨是两种单质,而不是原子,故不是同位素,故C错误;
D、分子式相同而结构不同的化合物互成同分异构体,而 和
和 的分子式和结构均相同,故为同一种物质,故D错误.
的分子式和结构均相同,故为同一种物质,故D错误.
故选B.
点评 本题考查了四同概念的辨析,难度不大,掌握概念的要点和描述对象是关键,注意掌握基础.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
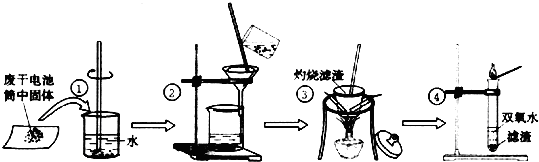
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中,加入硝酸酸化的硝酸银溶液 | 产生白色沉淀 | 含有Cl- |
| 2.检验NH4+ | 取少许滤液于试管中,加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 | 石蕊试纸变蓝色 | 含有NH4+ k |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
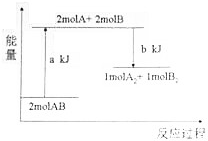
| A. | 该反应是放热反应 | |
| B. | 该反应一定要在加热条件下才能进行 | |
| C. | 断开lmolA2中的化学键和lmolB2中的化学键需吸收akJ的能量 | |
| D. | 1moIA2和1moIB2的总能量高于2molAB的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,1L0.3mol•L-1CH3COOH溶液和3L0.1 mol•L-1CH3COOH溶液中的H+数 | |
| B. | 纯水在25℃和80℃时的pH | |
| C. | 在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数 | |
| D. | 相同条件下,H2分别与Cl2、F2反应的反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 质量比为11:8 | B. | 原子个数之比为2:3 | ||
| C. | 物质的量之比为3:2 | D. | 密度之比为8:11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com