



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ���Ϻ���ʮ��У2012������ڶ���������ѧ���� ���ͣ�021
|
��������20 mL��0.1 mol��L��1��Na2CO3��Һ���μ���0.1 mol/L��HC1��Һ40 mL����Һ��pH���ͣ�����˵����ȷ����(NA��ʾ�����ӵ�����) | |
A�� |
��ȫ��Ӧ�Ժ���Һ�������� |
B�� |
���������20 mLʱ����Һ��NHCO3�����ʵ���Ϊ0.002NA |
C�� |
20 mL��0.1 mol��L��1��Na2CO3��Һ��c(Na+)��c(H+)��2c(CO |
D�� |
20 mL��0.1 mol��L��1��Na2CO3��Һ��c(H+)��2c(H2CO3)��c(HCO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������м���һ��2011��2012ѧ��߶���ѧ�ڵ������¿���ѧ���� ���ͣ�022
| |||||||||||||||||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

(2)��֪
B.Ksp(CaF2)������Ӻͷ�����Ũ�ȵ����������
C.����ϵ����û�г�������
D.����ϵ�����г�������
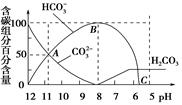
(3)��������20 mL 0.1 mol��L-1Na2CO3��Һ����μ���0.1 mol��L-1 HCl��Һ40 mL����Һ�к�̼Ԫ�صĸ�����(��CO2���ݳ���δ��)���ʵ�������(����)����ҺpH(����)�仯���������ͼ��

�������ͼ��ʾ�ش��������⣺
����ͬһ��Һ�У�H2CO3��![]() ��
��![]() (��ܡ����ܡ�) _________________�������档
(��ܡ����ܡ�) _________________�������档
�ڵ�pH=7ʱ����һ����ѧ����ʽ��ʾ��Һ�и������ӵ����ʵ���Ũ��֮��ĵ�����ϵ��_________________��
����֪��![]() (aq)ˮ�ⷴӦ��ƽ�ⳣ����
(aq)ˮ�ⷴӦ��ƽ�ⳣ����
Kh=![]() =2��10-4 mol��L-1
=2��10-4 mol��L-1
����Һ��c(![]() )��c(
)��c(![]() )=2��1ʱ����Һ��pH=_________________��
)=2��1ʱ����Һ��pH=_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���Ĵ�ʡ�߿���Ӧ���ԣ�һ�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������20 mL 0.1 mol/L Na2CO3��Һ���μ���0.1 mol/L HCl��Һ40 mL����Һ��pH���ͣ���ʱ��Һ�к�̼Ԫ�ص������ʵ���Ũ�ȵİٷֺ���(����)Ҳ�����仯(CO2���ݳ�δ����)����ͼ��ʾ������˵������ȷ����
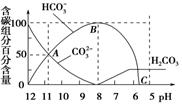
A��0.1 mol/L Na2CO3��Һ��c(OH��)��c(H��)��2c(H2CO3)��c(HCO3��)
B����A��c(Na��)��c(CO32��)��c(HCO3��)��c(OH��)��c(H��)��
C��������CO2������Һ��pHԼΪ5.6
D��0.05 mol/L NaHCO3��Һ��pH��8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���Ĵ�ʡ�ɶ�������ѧ�߿���Ӧ���ԣ�һ�������ۺϻ�ѧ�Ծ����������� ���ͣ���ѡ��
��������20 mL 0.1 mol/L Na2CO3��Һ���μ���0.1 mol/L HCl��Һ40 mL����Һ��pH���ͣ���ʱ��Һ�к�̼Ԫ�ص������ʵ���Ũ�ȵİٷֺ���(����)Ҳ�����仯(CO2���ݳ�δ����)����ͼ��ʾ������˵������ȷ����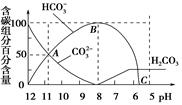
| A��0.1 mol/L Na2CO3��Һ��c(OH��)��c(H��)��2c(H2CO3)��c(HCO3��) |
| B����A��c(Na��)��c(CO32��)��c(HCO3��)��c(OH��)��c(H��)�� |
| C��������CO2������Һ��pHԼΪ5.6 |
| D��0.05 mol/L NaHCO3��Һ��pH��8 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com