
����Ŀ��2004������ʥ·��˹��ѧ������һ�����͵��Ҵ���أ����û� ���������ܼ�����200��C����ʱ���磬�Ҵ���رȼ״����Ч�ʸ߳�32���Ҹ���ȫ������ܷ�ӦΪ��C2H5OH+3O2�T2CO2+3H2O�����ʾ����ͼ������˵������ȷ���ǣ� �� 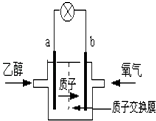
A.a��Ϊ��صĸ���
B.��ع���ʱ������b���ص��߾������ٵ�a��
C.��ع���ʱ��1mol�Ҵ�����ԭʱ����6mol����ת��
D.��������ĵ缫��ӦΪ��4H++O2+4e����2H2O
 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ������������ֵ������������ȷ���ǣ� ��
A.��״���£�33.6L�������к��з�ԭ�ӵ���ĿΪ1.5NA
B.3mol����������ˮ������ַ�Ӧ��ת��8NA������
C.50mL18.4molL��1Ũ����������ͭ�ȷ�Ӧ������SO2���ӵ���ĿΪ0.46NA
D.ij�ܱ�����ʢ��0.1molN2��0.3molH2 �� ��һ�������³�ַ�Ӧ��ת�Ƶ��ӵ���ĿΪ0.6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ӽ������ۼ��ĸ��������У�˵����ȷ���ǣ� ��
A.�����ӻ������У�ֻ�������Ӽ���û�й��ۼ�
B.�Ǽ��Լ�ֻ������˫ԭ�ӵĵ��ʷ�����
C.�ڹ��ۻ���������ڣ�һ�����������Ӽ�
D.�ɲ�ͬԪ����ɵĶ�ԭ�ӷ����һ��ֻ���ڼ��Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧԭ����ʾ�˲�ͬ��������ˮ��Һ���в�ͬ����Ϊ���밴Ҫ��ش��������⣺����֪��H2SO3�� Ka1=1.7��10��2��Ka2=6.0��10��8 �� NH3��H2O��Kb=1.8��10��5��
��1���������ʵ�����SO2��NH3����ˮ��ַ�Ӧ��������Һ��_________�ԣ�����Һ�и�����Ũ���ɴ�С��˳��Ϊ��_____________________________________________,������Һ��c��H+���� c��OH����=___________________________����д����ʽ��

��2����NaOH��Һ���������е�SO2�������õ�Na2SO3��Һ���е�⣬��ѭ������NaOH��ͬʱ�õ�H2SO4����ԭ������ͼ��ʾ���缫����Ϊʯī����
�� ͼ��a��Ҫ���ӵ�Դ��(����������������)________����C��������������________��
��SO32���ŵ�ĵ缫��ӦʽΪ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д����ȷ����
A. �Ȼ��������ۣ�Fe 3+ ��Fe === 2Fe2+
B. ��������ˮ��2Na �� 2H2O === 2Na+ �� 2OH�� �� H2��
C. ϡ������̼��ƣ�CaCO3 �� 2H�� === Ca2+ �� CO2 �� �� H2O
D. ͭ��Ũ���Cu �� 4H���� 2NO3�� ![]() Cu2����2NO2�� ��2H2O
Cu2����2NO2�� ��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na2O2��CO2�ķ�Ӧ�У��������뻹ԭ������������( )
A. 1��1 B. 2��1 C. 1��2 D. 8��53
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж��������йػ�ѧ����ķ�����ȷ���ǣ�������
A.�ƺ����������ں����ḻ�Ŀ���Ԫ�أ����Ƕ�������Ԫ��
B.�������պͷ��缼���Ľ�ϣ��Ƚ������Ⱦ���⣬����Ч��������������������
C.������ͨ��������Ҫ��Ӧԭ��֮һΪ��CaO+SiO2 ![]() =CaSiO3
=CaSiO3
D.��ù�������緢�ֵ���Ȼ�����أ��������������õ���ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z�����ֳ����Ķ���������Ԫ�أ���ԭ�Ӱ뾶��ԭ�������ı仯��ͼ��ʾ����֪Y��Z����Ԫ�صĵ����ǿ�������Ҫ�ɷ֣�Wԭ�ӵ�������������Neԭ�ӵ��������������1����ش���������:

(1)����Ԫ�ص����л��ϼ��У�������ϼ�Ϊ______�ۣ���������ϼ�Ϊ_____�ۡ�
(2)���ҷֱ�����W��X��Y��Z����Ԫ���е�����Ԫ����ɵij���������������������ɱ�����ã��仯ѧʽΪ_________������������һ�����ӻ�������������ʣ��仯ѧʽΪ________��
(3)HYO3�����Ա�HWOǿ�����˾ݴ���ΪY�ķǽ�����ǿ��W������Ϊ���ֿ����Ƿ���ȷ��˵������:____________________��
(4)Ԫ��Y��W���γ�һ�ֻ�����YW3��YW3�ܷ���ˮ�ⷴӦ����һ�������һ�����ᣬд���÷�Ӧ�Ļ�ѧ����ʽ:________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�������ǿ�ᷴӦ��������ǿ�Ӧ����( )
A.Ba(OH)2B.CaOC.Al(OH)3D.NaCl
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com