
| A、锌电极为负极 |
| B、锌电极为正极 |
| C、反应中Zn被氧化 |
| D、反应中Zn被还原 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
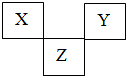 X、Y、Z是VA→VIIA族的三种短周期元素,他们在周期表中的位置如图所示.
X、Y、Z是VA→VIIA族的三种短周期元素,他们在周期表中的位置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盛放氢氧化钠溶液的试剂瓶用橡皮塞,不用玻璃塞 |
| B、常温下可用铁、铝制容器盛放浓硫酸或浓硝酸,因为它们不反应 |
| C、N2和H2合成NH3,属于氮的固定 |
| D、丁达尔效应是检验胶体和溶液的一种常用方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用催化剂不改变反应速率 |
| B、改变温度对反应速率无影响 |
| C、升高温度能加快反应速率 |
| D、使用催化剂能加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A、A电极是负极 |
| B、外电路中电子由B电极通过导线流向A电极 |
| C、产物为无污染的水,属于环境友好电池 |
| D、该电池的总反应:2H2+O2═2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 滴定前读数 | 滴定末读数 | ||
| 1 | 20.00 | 0.50 | 31.50 |
| 2 | 20.00 | 1.00 | 32.04 |
| 3 | 20.00 | 1.10 | 32.18 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com