
【题目】[2016·北京]用石墨电极完成下列电解实验。下列对实验现象的解释或推测不合理的是
实验一 | 实验二 | |
装置 |
|
|
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生;…… |
A.a、d处:2H2O+2e![]() H2↑+2OH
H2↑+2OH
B.b处:2Cl2e![]() Cl2↑
Cl2↑
C.c处发生了反应:Fe2e![]() Fe2+
Fe2+
D.根据实验一的原理,实验二中m处能析出铜
【答案】B
【解析】本题结合实验考查电化学知识,意在考查考生对电解池的熟练程度和分析能力。由于有外接电源,所以实验一和实验二均为电解池装置。实验一中,铁丝中的电流方向为从d到c,电子移动方向为从c到d,所以实验一的装置是比较复杂的电解池,其中a为阴极,c为阳极,d为阴极,b为阳极。a、d处发生反应2H2O+2e![]() H2↑+2OH,A项正确;若b处发生反应2Cl2e
H2↑+2OH,A项正确;若b处发生反应2Cl2e![]() Cl2↑,不足以解释b处“变红”和“褪色”现象,故B项错误;c处铁作阳极,发生反应Fe2e
Cl2↑,不足以解释b处“变红”和“褪色”现象,故B项错误;c处铁作阳极,发生反应Fe2e![]() Fe2+,由于生成的Fe2+浓度较小,且pH试纸本身有颜色,故颜色上无明显变化,C项正确;实验二是一个更加复杂的电解池装置,两个铜珠的左端均为阳极,右端均为阴极,初始时两个铜珠的左端(阳极)均发生反应Cu2e
Fe2+,由于生成的Fe2+浓度较小,且pH试纸本身有颜色,故颜色上无明显变化,C项正确;实验二是一个更加复杂的电解池装置,两个铜珠的左端均为阳极,右端均为阴极,初始时两个铜珠的左端(阳极)均发生反应Cu2e![]() Cu2+,右端(阴极)均发生反应2H++2e
Cu2+,右端(阴极)均发生反应2H++2e![]() H2↑,一段时间后,Cu2+移动到m和n处,m、n处附近Cu2+浓度增大,发生反应Cu2++2e
H2↑,一段时间后,Cu2+移动到m和n处,m、n处附近Cu2+浓度增大,发生反应Cu2++2e![]() Cu,m、n处能生成铜,D正确。
Cu,m、n处能生成铜,D正确。


科目:高中化学 来源: 题型:
【题目】在具有下列电子排布式的原子中,原子半径最大的是( )
A. 1s22s22p63s23p1 B. 1s22s22p1 C. 1s22s22p3 D. 1s22s22p63s23p4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为________(填化学式)。
(2)KClO4是助氧化剂,其中含有化学键的类型为________________________。
(3)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
________________________________________________________________。
(4)NaN3是气体发生剂,受热分解产生N2和Na。取56 g上述产气药剂,分解产生的气体通过碱石灰后的体积为16.8 L(标准状况),该产气药剂中NaN3的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)硫铁矿烧渣用稀硫酸酸溶时的不溶物为 (填化学式)。
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有 ;
步骤Ⅳ中应选用 试剂调节溶液的pH(填字母编号)。
A.稀硝酸 | B.氢氧化钠溶液 | C.高锰酸钾溶液 | D.氨水 |
(3)检验步骤Ⅲ已经进行完全的试剂是 。
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是 。
(5)步骤Ⅵ在空气中煅烧发生反应的化学反应方程式为 。
(6)欲测定硫铁矿烧渣中Fe元素的质量分数,称取ag样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg。
①写出加入足量的H2O2发生反应的离子反应方程式 ;
②测得该样品中Fe元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,全国特大“地沟油”案件宣判大快人心.“地沟油”中含有大量的油脂,油脂是多种高级脂肪酸的甘油酯.下列说法不正确的是
A.通过适当方法,可将“地沟油”用于生产燃料
B.地沟油有毒,不能回收利用,只能排入下水道
C.地沟油在碱性条件下可水解为甘油和高级脂肪酸盐
D.地沟油可用作化工原料,如生产肥皂等产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)为白色粉末,容易吸水潮解,可溶于异丙胺(熔点:-101℃,沸点:33℃),在干空气中稳定,在湿空气中分解,是无机合成和有机合成中常用的选择性还原剂。某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
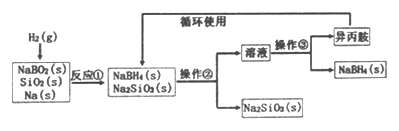
下列说法不正确的是
A. 反应①的化学方程式为 NaBO2+2SiO2+4Na+2H2=NaBH4+2Na2SiO3
B. 反应①加料之前需将反应器加热至100℃以上并通入氩气
C. 操作②、操作③分别是过滤与蒸发结晶
D. NaBH4在水溶液中分解的离子方程式BH4-+2H2O=BO2-+4H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________。
(4)相同条件下,体积比为1∶2和质量比为1∶2的H2和O2的混合气体,其物质的量之比分别是________和________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中出现了“增铁酱油”、“高钙奶粉”、“富硒茶叶”、“含氟牙膏”、“加碘食盐”等商品。这里的铁、钙、硒、氟、碘应理解为 ( )
A. 元素 B. 分子 C. 氧化物 D. 单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com