
【题目】已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=xkJ·mol–1,不同条件下反应过程能量变化如图所示。下列说法中不正确的是( )
2SO3(g) ΔH=xkJ·mol–1,不同条件下反应过程能量变化如图所示。下列说法中不正确的是( )

A.反应的ΔH<0
B.过程b使用了催化剂
C.使用催化剂可以提高SO2的平衡转化率
D.过程b发生两步反应,第一步为吸热反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇时,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1= -99kJmol-1
CH3OH(g) △H1= -99kJmol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2= 58kJmol-1
CH3OH(g)+H2O(g) △H2= 58kJmol-1
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3=+41kJmol-1
CO(g)+H2O(g) △H3=+41kJmol-1
(1)一定温度下,向体积为2L的密闭容器中加入CO和H2,假设只发生反应①,达平衡后测得各组分浓度如下:
物质 | CO | H2 | CH3OH |
浓度(molL-1) | 0.9 | 1.0 | 0.6 |
①列式并计算平衡常数K=___。
②若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是___。
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正__v逆(填“>”、“<”或“=”)。
(2)在实际生产中,当合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α(CO)与温度和压强的关系如图所示。
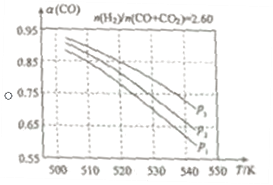
α(CO)值随温度升高而___(填“增大”或“减小”),其原因是___。图中的压强由大到小为___,其判断理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应在某体积为5L的密闭容器中进行,在从0~3分钟各物质的量的变化情况如图所示(A、B、C均为气体)
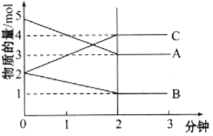
(1)该反应的化学方程式为__________________。
(2)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是___________(填字母)。
A.气体总质量保持不变 B.A、B、C的浓度都相等
C.A、B、C的浓度不再发生变化 D.A、B、C的分子数之比为2:1:2
E.正反应和逆反应都已停止 F.容器内气体密度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应原理的应用叙述中,正确的是![]()
A.用明矾净水是因为![]() 水解生成的
水解生成的![]() 胶粒具有较强的吸附性
胶粒具有较强的吸附性
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀
D.为了防止钢铁锈蚀,把输油管的铸铁管连接外加直流电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物1是一种常见的植物两味油,常用脂肪烃A和芳香烃D按如下路线合成:

已知:①R1CHO+R2CH2CHO![]()

![]()

②通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1)A的名称是___,H含有的官能团名称是_____。
(2)②的反应条件是___。⑦的反应类型是______。
(3)I的结构简式是________。
(4)④的化学方程式是_________。
(5)L是I的同分异构体且含有相同官能团,其结构中苯环上只有两个处于对位的取代基,则L共有_种(不考虑立体异构)
(6)参照以上合成路线,设计以C为原料制备保水树脂 的合成路线(无机试剂任选)__ 。
的合成路线(无机试剂任选)__ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应N2(g)+3H2(g)![]() 2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
A.3v (N2)正=v (H2)正
B.v (N2)正=v (NH3)逆
C.v (N2)正=3v (H2)逆
D.2v (H2)正=3v (NH3)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶无色澄清的溶液,其中可能含NH4+、K+、Na+、Mg2+、H+、Cu2+、CO32-、I-中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,发现溶液呈强酸性。
②取部分溶液,逐滴加入NaOH稀溶液,使溶液逐渐从酸性转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成。
③将②得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实回答下列问题:
(1)在溶液中,肯定存在的离子有________,肯定不存在的离子有________,不能确定是否存在的离子有________。
(2)写出实验③中的离子方程式:___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图中的实验方案,能达到实验目的的是 ( )
A.验证FeCl3对H2O2分解反应有催化作用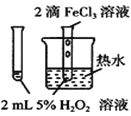
B.探究温度对平衡2NO2![]() N2O4的影响
N2O4的影响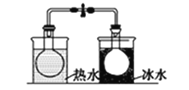
C.除去CO2气体中混有的SO2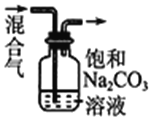
D.比较HCl、H2CO3和H2SiO3的酸性强弱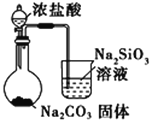
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )

A. ①为简单立方堆积 ②为六方最密堆积 ③为体心立方堆积 ④为面心立方最密堆积
B. 每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C. 晶胞中原子的配位数分别为:①6,②8,③8,④12
D. 空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com