
����Ŀ����һƿ��ɫ�������Һ�����п��ܺ�NH4+��K����Na����Mg2����H����Cu2����CO32-��I���е�һ�ֻ��֣�ȡ����Һ��������ʵ�飺
����pH��ֽ���飬������Һ��ǿ���ԡ�
��ȡ������Һ����μ���NaOHϡ��Һ��ʹ��Һ������ת��Ϊ���ԣ��ڵμӹ����м��μ���Ϻ���Һ�о��������ɡ�
�۽��ڵõ��ļ�����Һ���ȣ�������ų�����������ʹʪ��ĺ�ɫʯ����ֽ������
��������ʵ����ʵ�ش��������⣺
��1������Һ�У��϶����ڵ�������________���϶������ڵ�������________������ȷ���Ƿ���ڵ�������________��
��2��д��ʵ����е����ӷ���ʽ��___________________________________________________��
���𰸡�![]() ��H����I�� Mg2����Cu2����
��H����I�� Mg2����Cu2����![]() K����Na��
K����Na�� ![]()
��������
��ɫ��Һ��һ����������ɫ��Cu2+��
����pH��ֽ���飬������Һ��ǿ���ԣ���һ�����ڴ�����H+��̼��������������ӷ�Ӧ������һ��������![]() ��������Һ�������ж�һ�����ڵ����ӣ�
��������Һ�������ж�һ�����ڵ����ӣ�
����ȡ������Һ����μ���ϡNaOH��Һ��ʹ��Һ��������ת��Ϊ���ԣ��ڵμӹ����м��μ���Ϻ���Һ�о��������ɣ���һ��������Mg2+��
�۽��ڵõ��ļ�����Һ���ȣ�������ų�����������ʹʪ��ĺ�ɫʯ����ֽ������������Ϊ��������һ������![]() ��
��
����Һ���Ƿ���K����Na������ȷ�����������Ϸ������н��
��1����������������֪���϶����ڵ������У�![]() ��H����I�����϶������ڵ������У���Mg2����Cu2����
��H����I�����϶������ڵ������У���Mg2����Cu2����![]() ������ȷ���Ƿ���ڵ������У�K����Na����
������ȷ���Ƿ���ڵ������У�K����Na����
��2��ʵ���Ϊ![]() ��OH-��Ӧ�ڼ��������²��������ķ�Ӧ���䷴Ӧ���ӷ���ʽΪ��
��OH-��Ӧ�ڼ��������²��������ķ�Ӧ���䷴Ӧ���ӷ���ʽΪ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������AlCl3��MgSO4�����Һ�������в��ϼ���NaOH��Һ���õ��������������NaOH��Һ�������ͼ��ʾ��ԭ��Һ��Cl����SO42-�����ʵ���֮��Ϊ �� ��

A.1��3B.2��3
C.6��1D.3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���һ��ȼ�ϵ�أ���ͼ��ʾ����Ŀ����̽���ȼҵԭ���ʹ�ͭ�ľ���ԭ����������װ����XΪ�����ӽ���Ĥ��
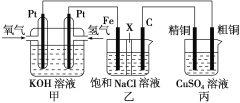
����Ҫ��ش�������⣺
��1��ͨ�������ĵ缫Ϊ____������������������������ĵ缫��ӦʽΪ____________________________��
��2��ʯī�缫Ϊ____�����������������������Ӧһ��ʱ�������װ���е����̪��Һ��____�����������ʯī������������Һ�ȱ�졣
��3�������ͭ�к���п���������ʣ���װ���з�Ӧһ��ʱ�䣬����ͭ��ҺŨ�Ƚ�____���������С�����䡱������ͭ�缫�ϵĵ缫��ӦʽΪ______________________________________��
��4��д�������������ҳص����ܷ�Ӧ����ʽ��_________________________��
��5������������׳������ı�״���µ�����11.2 L���������������Ӧ����ͭ������Ϊ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2SO2(g)+O2(g)![]() 2SO3(g) ��H=xkJ��mol�C1����ͬ�����·�Ӧ���������仯��ͼ��ʾ������˵���в���ȷ���ǣ� ��
2SO3(g) ��H=xkJ��mol�C1����ͬ�����·�Ӧ���������仯��ͼ��ʾ������˵���в���ȷ���ǣ� ��

A.��Ӧ����H��0
B.����bʹ���˴���
C.ʹ�ô����������SO2��ƽ��ת����
D.����b����������Ӧ����һ��Ϊ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������������(NH2COONH4)�����ܱ������У�������ӦNH2COONH4(s)![]() 2NH3(g)��CO2(g)���÷�Ӧ��ƽ�ⳣ���ĸ�����(��lgK)ֵ���¶�(T)�ı仯������ͼ��ʾ������˵������ȷ����
2NH3(g)��CO2(g)���÷�Ӧ��ƽ�ⳣ���ĸ�����(��lgK)ֵ���¶�(T)�ı仯������ͼ��ʾ������˵������ȷ����

A. �÷�Ӧ����H>0
B. NH3�������������ʱ���÷�Ӧһ���ﵽƽ��״̬
C. A���Ӧ״̬��ƽ�ⳣ��K(A)��10��2.294
D. 30��ʱ��B���Ӧ״̬��v(��)<v(��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����£�����ʵ����������������۲�������ǣ� ��
ѡ�� | ���������� | ���� |
A | ��pH��ֽ���0.1mol/LCH3COOH��ҺpHԼΪ3 | CH3COOH��������� |
B | ��ij��ɫ��Һ�м�������ϡ���ᣬ������ɫ��ζ���壻�ٽ�������ͨ�����ʯ��ˮ��������ɫ���� | ��Һ�п��ܺ���CO |
C | ��pH�Ʋⶨ��ͬŨ�ȵ�CH3COONa��Һ��NaClO��Һ��pH��ǰ�ߵ�pHС�ں��ߵ� | HClO����������CH3COOH |
D | ��2mL1mol/LNaOH��Һ�м���1mL0.1mol/LMgCl2��Һ��������ɫ�������ټ���1mL0.1mol/LFeCl3��Һ���������ɫ���� | Mg(OH)2����ת��ΪFe(OH)3���� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����(N2H4)ȼ�ϵ�صĽṹ��ͼ��ʾ������˵����ȷ���� (����)
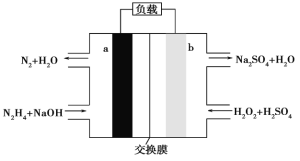
A.aΪ�������缫��ӦʽΪ��N2H4-4e-+4OH-=N2����4H2O
B.���·��ÿͨ��1mol ���ӣ�����NA��Na����������Ĥ�������ƶ�
C.b���ĵ缫��ӦʽΪH2O2+2e-=2OH-
D.�øõ������Դ��ⱥ��ʳ��ˮ�����õ�0.1mol Cl2ʱ������Ҫ����0.1mol N2H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ����
A.��֪0.1 mol��L��1�Ĵ�����Һ�д��ڵ���ƽ�⣺CH3COOH![]() CH3COO����H�����������ռ���Һ��ʹ��Һ��
CH3COO����H�����������ռ���Һ��ʹ��Һ��![]() ֵ����
ֵ����
B.25 ��ʱ����ˮ�м�����������CH3COONa��ˮ�ĵ���ƽ�⣺H2O![]() H����OH�������ƶ���c(H��)����
H����OH�������ƶ���c(H��)����
C.ȡc(H��)��0.01 mol��L��1������ʹ����100 mL���ֱ�ϡ��2�����ٷֱ����0.3 gп�ۣ�����ͬ�����³�ַ�Ӧ��������п��Ӧ�����ʴ�
D.����������Һ�еμ�ϡ����õ���pH��5�Ļ����Һ�У�c(Na��)��c(NO3�� )
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��ʵ����������ͼװ�ý����к��ȵIJⶨ���ش��������⣺
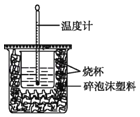
��1����ͼ����һ��δ����������_____�����������ƣ���
��2�������0.50 mol/L��������������ƹ������ʵ�飬����ݴ�ʵ���������д�к��ȵ��Ȼ�ѧ����ʽ�еġ�H��_____������ƫ������ƫС����������������ԭ����_____��
��3������50 mL 0.50 mol/L��ϡ������50 mL 0.55 mol/L��ϡ����������Һ����ʵ�飬����Һ���ܶȾ�Ϊ1 g/cm3���кͺ���Һ�ı�����c��4.18 J/��g�棩�������ʵ�����ݼ��㣬�к��ȡ�H��_____ ��ȡС�����һλ����
ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | ||
���� | NaOH | ƽ��ֵ | ||
1 | 26.2 | 26.0 | 26.1 | 29.4 |
2 | 27.0 | 27.4 | 27.2 | 31.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
��4��������3���еĽ�����к��ȵ�����ֵ��ƫ�����ƫ���ԭ�������_____
a��ʵ��װ�ñ��¡�����Ч����
b��ʹ�û��β�����������裬ʹ���ַ�Ӧ
c���ֶ�ΰ�NaOH��Һ����ʢ��ϡ�����С�ձ���
d�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�Ӳⶨ������Һ���¶�
������ijѧ����0.2000molL��1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ�����Ϊ���¼�����
��������ˮϴ�Ӽ�ʽ�ζ��ܣ�������ע��NaOH��Һ����0���̶�������
�ڹ���õζ��ܲ�ʹ�ζ��ܼ������Һ��
�۵���Һ������0������0���̶������£������¶���
����ȡ20.00mL����Һע��ྻ����ƿ�У�������3�η�̪��Һ
���ñ�Һ�ζ����յ㣬���µζ���Һ�������
��ش�
��1�����ϲ����д�����ǣ����ţ�_____���ô�������ᵼ�²ⶨ���������ƫ��������ƫС��������Ӱ������_____��
��2��������У��ڼ��µζ���Һ�����ʱ���ζ��ܼ��������ݣ������²ⶨ���������ƫ��������ƫС��������Ӱ������_____��
��3���жϵζ��յ�������ǣ�_____��
��4����ͼ��ij�εζ�ʱ�ĵζ����е�Һ�棬�����Ϊ_____mL��

��5�������������ݣ���������������Һ��Ũ�ȣ�_____��
�ζ����� | ���������mL�� | ���ռ������mL�� | |
�ζ�ǰ������mL�� | �ζ��������mL�� | ||
��һ�� | 20.00 | 0.30 | 20.40 |
�ڶ��� | 20.00 | 4.00 | 24.20 |
������ | 20.00 | 2.00 | 24.30 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com