
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑ + H2O
B. CaO+H2O=Ca(OH)2
C. CaCO3![]() CaO+CO2↑
CaO+CO2↑
D. 3Cu+8HNO3(稀) = 3Cu(NO3)2+2NO↑+4H2O
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】Cl2和SO2都具有漂白作用,能使品红溶液褪色。若将等物质的量的Cl2、SO2混合后再通入品红与BaCl2的混合溶液,能观察到的现象是( )
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①②B.①③C.②③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。据图判断错误的是
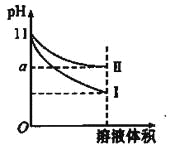
A. a的数值一定大于9
B. I为氢氧化钠溶液稀释时溶液的pH变化曲线
C. 完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V( NaOH)<V(氨水)
D. 稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属钠的叙述中,说法正确的是()
A.钠在空气中燃烧,发出黄色火焰B.钠在空气中燃烧,产物是Na2O
C.钠是银白色金属,硬度大,熔点高D.取用金属钠时,剩余的钠不能放回原瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于在密闭容器中的可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡状态时,4v正(O2)=5v逆(NO)
B. 当气体的平均相对分子质量不变时,反应达到平衡
C. 达到化学平衡状态时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 其他条件不变,增大体系压强,化学平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中的离子,能在溶液中大量共存的是( )
A.Na+、Mg2+、Cl﹣、OH﹣
B.H+、Ca2+、CO32﹣、NO3﹣
C.Cu2+、K+、SO42﹣、NO3﹣
D.Na+、H+、OH﹣、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铝在现代生产和日常生活中应用广泛。工业上用电解熔融氧化铝的方法来制取金属铝,纯净氧化铝的熔点很高(约2045℃),在实际生产中,通过加入助熔剂冰晶石(Na3AlF6)在1000℃左右就可以得到熔融体。反应方程式为2Al2O3![]() 4Al+3O2↑。
4Al+3O2↑。
(1)在电解时阴极的电极反应式_________________,阳极的电极反应式_____________________。
(2)对金属制品进行抗腐蚀处理,可延长其使用寿命,以铝材为阳极,在H2SO4溶液中电解,可使铝材表面形成氧化膜,阳极电极反应式为________________________。在电解过程中,阴极附近溶液的pH________(填“增大,减小或不变”)
(3)“863”计划和中科院“百人计划”支持的环境友好型铝碘电池已研制成功,电解质为AlI3溶液,已知电池总反应为2Al+3I2=2AlI3,该电池负极的电极反应为:_____________________________,当负极质量减少27g时,在导线有________个电子通过。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某烷烃完全燃烧后,生成的气体缓缓通过盛有0.5L 2mol / LNaOH溶液中,生成的 Na2CO3和NaHCO3的物质的量之比为1:3,则该烷烃为
A. 甲烷 B. 乙烷 C. 丙烷 D. 丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强.
⑴若剩余气体的体积是15 L,则原CO和H2的混合气体中V(CO)=________L,V(H2)=________L.
⑵若剩余气体的体积为a L,则原CO和H2的混合气体中V(CO)∶V(H2)=________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com