
| A. | 用铁作阴极 | B. | 用碳棒作正极 | ||
| C. | 食盐水从阳极区加入 | D. | 烧碱溶液从阴极区流出 |
分析 用有阳离子交换膜(只允许阳离子通过)的电解槽电解食盐水时,
A.Fe作阴极,阴极上氢离子放电生成氢气;
B.电解池电极为阴阳极,原电池电极为正负极;
C.阳极上氯离子放电生成氯气;
D.阴极上氢离子放电生成氢气,同时阴极附近有氢氧根离子生成.
解答 解:用有阳离子交换膜(只允许阳离子通过)的电解槽电解食盐水时,
A.Fe作阴极,阴极上氢离子放电生成氢气,同时阴极附近有氢氧化钠生成,所以铁电极不发生反应,故A正确;
B.电解池电极为阴阳极,原电池电极为正负极,所以石墨作阳极而不是正极,故B错误;
C.阳极上氯离子放电生成氯气,所以阳极区域应该加入含有氯离子的电解质溶液,加入氯化钠溶液即可,故C正确;
D.阴极上氢离子放电生成氢气,同时阴极附近有NaOH生成,所以烧碱溶液从阴极区流出,故D正确;
故选B.
点评 本题考查电解原理,为高频考点,明确各个电极上发生的反应是解本题关键,难点是确定各个电极附近加入物质流出物质,题目难度不大.


科目:高中化学 来源: 题型:选择题
 原电池原理的发现和各式各样电池装置的发明是化学对人类的一项重大贡献.关于如图
原电池原理的发现和各式各样电池装置的发明是化学对人类的一项重大贡献.关于如图| A. | 将电能转化为化学能的装置 | B. | 电子由铜片经导线流向锌片 | ||
| C. | 锌片为负极,发生氧化反应 | D. | 铜片上发生的反应为Cu2++2e-═Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
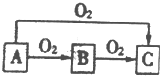 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物)
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
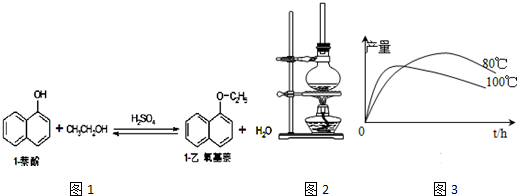
| 物质 | 相对分 子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
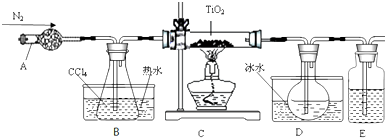
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫在少量氧气中燃烧成SO2,过量能生成SO3 | |
| B. | 铁丝在少量氯气中燃烧生成FeCl2,过量则生成FeCl3 | |
| C. | 氯水滴入淀粉碘化钾稀溶液中,少量氯水有蓝色,过量蓝色消失 | |
| D. | NaClO溶液中通少量CO2生成Na2CO3和HClO,过量生成NaHCO3和HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
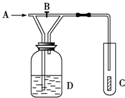 如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条上看不到明显现象;当关闭B阀后,C处红布逐渐褪色,则D瓶中装的是( )
如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条上看不到明显现象;当关闭B阀后,C处红布逐渐褪色,则D瓶中装的是( )| A. | 浓H2SO4 | B. | NaOH溶液 | C. | H2O | D. | 饱和NaCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com