
ʵ������18.4 mol��L-1��Ũ����������500mL 0.2 mol��L-1��ϡ���ᡣ
��1�������������˲��������ձ�����ͷ�ιܡ���Ͳ�⣬����Ҫ�ĸ�����������ɸ�ʵ�飬��д���� ��
��2����������Ũ��������Ϊ________ mL �����Т�10mL ��50mL ��100mL���ֹ�����Ͳ��Ӧ��ѡ��___________��������ţ�
��3��ʵ���������õ��������������÷ֱ��ǣ�___________��__________��
(4)���ж�����ƿ����ʹ�÷�������������ȷ����_____��
| A������ƿ�ϱ����ݻ����¶Ⱥ�Ũ�� |
| B������ƿ������ˮϴ�������� |
| C��������Һʱ�������õ�Ũ����С�ĵ�������ƿ�У���������ˮ���ӽ��̶��� 1��2 cm�������ý�ͷ�ιܼ�����ˮ���̶��� |
| D��ʹ��ǰҪ�������ƿ�Ƿ�©ˮ |
��1��500mL����ƿ��2��5.4 �٣�3������ ������4��D��5���٢�
���������������1������һ�����ʵ���Ũ����Һ��Ҫ������һ���������ƿ����ͷ�ιܡ���Ͳ���ձ���������������ƽ������2����Ũ�������ΪVmL��18.4��V��10-3=500��0.2��10-3,V=5.4mL��ѡ��10mL��Ͳ����3���ܽ�ʱ�ò��������衢ת��ʱ�ò�������������4������ƿ��û��Ũ�ȣ�����ƿ���غ�ɣ�����ֱ��������ƿ��������Һ������ƿʹ��ǰҪ��©����5��δϴ���ձ��Ͳ�������nƫС��cƫС��δ��ϡ�ͺ��������Һ��ȴ������VƫС��cƫ������ƿ������������ˮ��c��Ӱ�죻����ʱ���ӿ̶��ߣ�Vƫ��cƫС��
���㣺һ�����ʵ���Ũ����Һ������
��������д����ƿʱһ��Ҫ�й�������ʱ����c=n/V������Ũ��������ˮ���ȣ��ܽ������������Һת��������ƿ��


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| m |
| 233 |
| V |
| 200 |
| m |
| 233 |
| V |
| 200 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����������ʮ����2011������ڶ����¿���ѧ���� ���ͣ�058
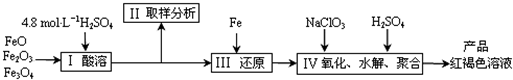
������������(��Ҫ�ɷ�Ϊ���������������SiO2)Ϊԭ����ȡ���߷����������ۺ�������(PFS)���仯ѧʽ[Fe2(OH)n(SO4)3��0.5n]m�㷺������ˮ��������ʵ���������£�

(1)ʵ������18.4 mol��L��1��Ũ��������250 mL��4.8 mol��L��1��������Һ�����õIJ����������ձ�����������������(һ���ܾ�ȷ��ȡһ�����Һ�������)�⣬����________��
(2)��������Ҫ��ѧ�ɷ���________
(3)����ҺX�м�����������ۺ���ˣ���Һ��Ũ�����ᾧ���Ƶ��̷����������ۺ�������Ҫ��Ӧ�����ӷ���ʽΪ________��
(4)��ҺY��pHӰ���Ʒ������������������pH��ֽ�ⶨ��ҺpH�IJ���������________������ҺY��pHƫС������PFS����������������ƫ________(��ߡ��͡�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡģ���� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪2KCl�����壩��H2SO4��Ũ��![]() K2SO4��2HCl������ʵ�����ø�ԭ����ȡHCl�ķ���װ����ʵ�������������������������ƣ���ͬ�����ƺ�HCl��������ˮ�������ᣬ����ʱ�õ��õ�©��������ʵ���� O2����KClO3Ϊԭ�ϣ�MnO2���������IJ���Ϊԭ�ϣ����Ƶ�HCl������ȡCl2��
K2SO4��2HCl������ʵ�����ø�ԭ����ȡHCl�ķ���װ����ʵ�������������������������ƣ���ͬ�����ƺ�HCl��������ˮ�������ᣬ����ʱ�õ��õ�©��������ʵ���� O2����KClO3Ϊԭ�ϣ�MnO2���������IJ���Ϊԭ�ϣ����Ƶ�HCl������ȡCl2��
��1��ijѧ�������ʵ�鲽�������ǣ��ܽ⡢�������ᾧ�������塣���л�ȱ�ٵı�Ҫ������������
��2��ijѧ�����е�ʵ����ƷΪ���ձ���Բ����ƿ����������Ͳ������ƿ����Һ©�����ƾ��ơ�ҩ�ס�������ƽ������̨�������С���Ȧ����˫����Ƥ�����������ܡ���Ƥ�ܡ��������ˮ����ȱ�ٵı�Ҫ�Լ��� ������������ ���� ����ȱ�ٵı�Ҫ��ʵ����Ʒ�������������������������������������� ����
��3��д���Ƶõ�HCl��Һ��MnO2��Ӧ��Cl2�����ӷ���ʽ���������������������������������� ��
��4����ͬѧ��51.33 g��MnO2������Ũ���Ṳ����ȡCl2������Ϊm g����ͬѧ��200 mL 36.5%��Ũ���ᣨ�ѣ�1.18 g/cm3����������MnO2������ȡCl2���õ�Cl2������Ϊn g��ɰ���Ƿ�Ӧ�����ĵ�ǰ���£�m��n�Ĵ�С��ϵ��m�� ��n���������������
��5�������Cl2���յ�װ�������õ������������������������� �����Լ��� ���� ��ѡ����ţ�A. NaOH������Һ��B. Ca(OH)2������Һ������ѡ����������� ����������������������������������������������������������������������������������������������������������������������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com