
【题目】下列实验中,所使用的装置(部分夹持装置略)、试剂和操作方法都正确的是 ( )
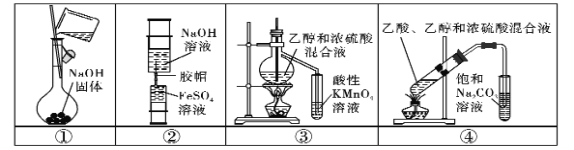
A.用装置①配制250 mL0.1 mol.L-1的NaOH溶液
B.用装置②制备少量Fe(OH)2固体
C.用装置③验证乙烯的生成
D.用装置④制取少量乙酸乙酯
科目:高中化学 来源: 题型:
【题目】常温下向20 mL浓度均为0.1 mol·L-1 NH4HSO4 、(NH4)2SO4混合溶液中逐滴加入0.1mol·L-1的Ba(OH)2溶液。充分反应后静置,Ba(OH)2溶液体积与溶液的pH的关系如下图,下列说法正确的是(假设过程中生成的NH3·H2O不分解)
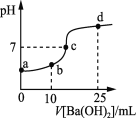
A.a点溶液中:c(NH4+)+c(NH3·H2O)=0.4 mol·L-1
B.b点溶液中:c(NH4+)>c(SO42-)>c(H+)>c(NH3·H2O)>c(OH-)
C.c点溶液中:c(Ba2+) + c(NH4+)=c(SO42-)
D.d点溶液中:c(NH3·H2O)>c(SO42-)>c(NH4+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列转化关系图,且知采用电解熔融氯化钠的方法可以生产金属钠:2NaCl(熔融)![]() 2Na+Cl2↑,下列说法不正确的是( )
2Na+Cl2↑,下列说法不正确的是( )

A.A、C、E一定含有同种元素B.若在B中点燃铜丝会产生棕黄色烟
C.C与D反应会产生红褐色沉淀D.D物质可能为FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na2S2O3)溶解,反应生成Na3[Ag(S2O3)2];在废定影液中加入Na2S使Na3[Ag(S2O3)2]中的银转化为Ag2S,并使定影液再生。将Ag2S在高温下转化为Ag,就达到了回收银的目的。
(1)铜、银、金在元素周期表中位于同一族相邻周期,基态铜原子的价电子排布式为___。
(2)Na、O、S简单离子半径由大到小的顺序为___。
(3)S2O32-离子结构如图所示,其中心硫原子的杂化轨道类型为___。
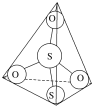
(4)Na3[Ag(S2O3)2]中存在的作用力有__。
A.离子键 B.共价键 C.范德华力 D.金属键 E.配位键
(5)在空气中灼烧Ag2S生成Ag和SO2,SO2分子中硫原子的价层电子对数为__,其分子空间构型为___。SO2易溶于水,原因是__。
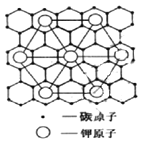
(6)SO2具有较强的还原性,碳与熔融金属钾作用,形成的晶体是已知最强的还原剂之一,碳的某种晶体为层状结构,钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图所示,则其化学式可表示为___。
(7)现在人们已经有多种方法来测定阿伏加德罗常数,X射线衍射法就是其中的一种,通过对金晶体的X 射线衍射图像的分析,可以得出金晶体的晶胞属于面心立方晶胞(与铜的晶胞相似)。若金原子的半径为am,金的密度为ρg·cm-3,金的摩尔质量为Mg·mol-1,试通过这些数据列出计算阿伏加德罗常数的算式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子方程式正确的是( )
A.稀硝酸和过量的铁屑反应:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.向Ca(
HCO3)
2溶液中加入过量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.碳酸氢钠溶液水解的离子方程式:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述,不正确的是
A. 正戊烷、异戊烷、新戊烷的沸点依次降低
B. 相对分子质量为104的烃,分子中不可能只存在单键
C. 光照下2,2一二甲基丙烷与Br2反应其二溴取代物有两种
D. FeCl3溶液可以把4种无色溶液:乙醇、苯酚、AgNO3溶液、KOH溶液一一区分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A-F 为中学化学常见物质,它们的焰色试验均为黄色。其中 A 为单质, B 与 C的组成元素相同,且 B 为淡黄色固体; D、 E、 F 的溶液均显碱性,其中 E 和 F 属于盐且相同物质的量浓度的溶液, E溶液的碱性更强。它们之间的相互转化关系如下图。(“![]() ”表示进一步反应即可转化,部分反应物、生成物和反应条件已略去)
”表示进一步反应即可转化,部分反应物、生成物和反应条件已略去)
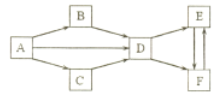
请回答下列问题:
(1)写出下列物质的化学式: B___, C___, E___。
(2)A![]() D 的化学方程式是_______________________。
D 的化学方程式是_______________________。
(3)B![]() D 的化学方程式是_______________________。
D 的化学方程式是_______________________。
(4)区分 E 和 F 两种固体的方法是:分别取等量的 E 和 F 两种固体少许于试管中,具体的操作现象和结论是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】8.8g FeS与400mL 1 mol/L硝酸溶液恰好完全反应,反应后产物为Fe2(SO4)3和Fe(NO3)3, X、H2O,则X为( )
A.N2B.NOC.N2OD.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物在冬季来临过程中,随着气温的逐渐降低,体内发生了一系列适应低温的生理生化变化,抗寒力逐渐增强。下图为冬小麦在不同时期含水量和呼吸速率变化关系图,据图推断错误的是
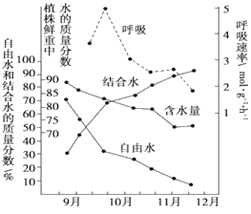
A. 结合水与自由水含量的比值,与小麦的抗寒性呈正相关
B. 总含水量下降是因为细胞呼吸增强,需要消耗更多的水
C. 随着气温和土壤温度的下降,小麦的含水量下降
D. 11月时,小麦细胞中含量最多的化合物仍是水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com