

 ��
��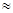 7.4���������������ѪҺ��ʱ��ѪҺ������ϵ�е�c(H+)/c(H2CO3)���ս� ��
7.4���������������ѪҺ��ʱ��ѪҺ������ϵ�е�c(H+)/c(H2CO3)���ս� ��| A����� | B����С | C���������� | D�����ж� |
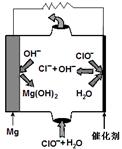
 CH3OH(g) +H2O(g) ��H ��
CH3OH(g) +H2O(g) ��H ��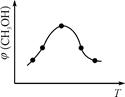
| �� �� | �� | �� |
| ��Ӧ�� Ͷ���� | 1molCO2 3molH2 | a molCO2��b molH2�� c molCH3OH(g)��c molH2O(g) |
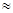 10-6���۹������Ậ�д�����H+�����c(H+)/c(H2CO3)���ս����
10-6���۹������Ậ�д�����H+�����c(H+)/c(H2CO3)���ս����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Cl2��SO2����ʹƷ����Һ��ɫ��˵�����߾��������� |
| B������Һ�еμ��ữ��Ba(NO3)2��Һ���ְ�ɫ������˵������Һ��һ����SO42�� |
| C��Fe��ϡHNO3��ϡH2SO4��Ӧ�������ݲ�����˵��Fe��������������û���Ӧ |
| D���ֱ����HCl��NH3����ƿ������ˮ�к�Һ���Ѹ��������˵�����߾�������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
 �������װ�øĽ��Ĵ�ʩ�����ɣ�
�������װ�øĽ��Ĵ�ʩ�����ɣ� �ٴ�ʩ����A��B֮���һ������ܣ�
�ٴ�ʩ����A��B֮���һ������ܣ� ����_______________________________________��
����_______________________________________�� �ڴ�ʩ��Ϊȷ��C�е�ʵ������������B��C֮���һ��װ��_________________��ϴ��ƿ��
�ڴ�ʩ��Ϊȷ��C�е�ʵ������������B��C֮���һ��װ��_________________��ϴ��ƿ�� ����_______________________��
����_______________________��| ʵ����� | Ԥ����������� |
| ����1��ȡ������ɫ�������Թܣ����� �����ϵ������������ɵ�����ͨ�� �� | �� ��˵����ɫ���庬��Na2SO3���� �������������� �� ������ |
| ����2���ڲ���1��Ӧ�����Һ���� �� | �� ����˵����ɫ���庬Na2SO4�� ��ϲ���1�Ľ��ۣ��� ���������������� �� ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
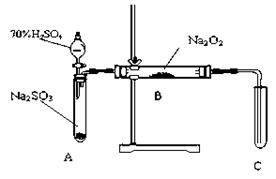
 B
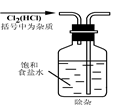
B 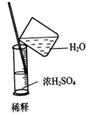 C
C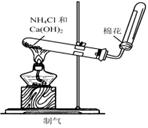 D��
D��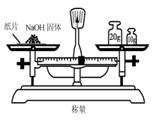
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | ʵ��Ŀ�� | �� �� |
| | �Ƚ�ˮ���Ҵ����ǻ���Ļ�����ǿ�� | �ý����Ʒֱ���ˮ���Ҵ���Ӧ |
| | ��֤����Һ�к���SO42- | ���������ữ�����ᱵ��Һ |
| | ��֤����Һ�к���S2- | ȡ������Һ���ڴ���Ǧ��ֽ�Ͽ��Ƿ��� |
| | ֤��SO2����Ư���� | ��SO2ͨ������KMnO4��Һ�� |
| | �Ƚ�ȷ��ͭ��þ�Ľ������ǿ�� | ��Pt���缫���Mg(NO3)2��Cu( NO3)2���Һ |
| | ȷ��̼����Ԫ�طǽ�����ǿ�� | ��ͬ��ͬŨ��Na2CO3��Na2SiO3ˮ��Һ��PH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
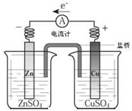
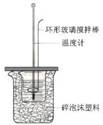
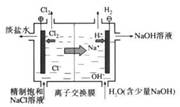

| A��ͭпԭ��� | B���к��Ȳⶨװ�� | C�����ӽ���Ĥ�����ԭ�� | D��������ȡװ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����



�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
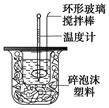
| �¶� ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | �¶Ȳ�ƽ��ֵ(t2��t1)/�� | ||
| H2SO4 | NaOH | ƽ��ֵ | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 3 | 26.4 | 26.2 | 26.3 | 29.8 | |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com