
【题目】下面是第二周期部分元素基态原子的电子排布图,据此下列说法一定错误的是( )
B C
C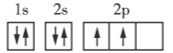
N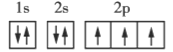 O
O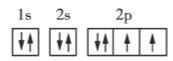
A.每个原子轨道里最多只能容纳2个电子
B.电子排在同一能级的不同轨道上时,总是优先单独占据一个轨道
C.每个能层所具有的能级数等于能层序数
D.若一个原子轨道里有2个电子,则其自旋状态相同
【答案】D
【解析】
观察题中四种元素的电子排布图可知,每个原子轨道里,最多能容纳2个自旋相反的电子,此即泡利原理;当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,而且自旋方向相同,此即洪特规则。
A. 由题给的四种元素原子的电子排布式可知,在一个原子轨道里,最多能容纳2个自旋相反的电子,A选项正确;
B. 由题给的四种元素原子的电子排布式可知,电子排在同一能级的不同轨道时,总是优先单独占据一个轨道,B选项正确;
C. 由题给的四种元素原子的电子排布式可知,任意能层的能级总是从s能级开始,而且能级数等于该能层序数,故C正确;
D. 由题给的四种元素原子的电子排布式可知,若一个原子轨道里有2个电子,则其自旋状态相反,D选项错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】(1)按系统命名法命名。
①CH3CH(C2H5)CH(CH3)2:_______________________________。
②CH3CH(CH2CH3)CH(CH2CH3)CH2CH(CH3)2:____________________。
③CH3CH(CH3)CH(CH2CH3)C(CH3)3:__________________________________。
(2)写出下列各种有机物的结构简式:
①2,3-二甲基-4-乙基己烷:________________________________。
②支链只有一个乙基且相对分子质量最小的烷烃:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PCl3和PCl5能发生如下水解反应:PCl3+3H2O→H3PO3+3HCl;PCl5+4H2O→H3PO4+5HCl,现将一定量的PCl3和PCl5混合物溶于足量水中,在加热条件下缓缓通入0.020molO2,恰好将H3PO3氧化为H3PO4。往反应后的溶液中加入15.725gCa(OH)2,充分反应后磷元素全部转化为Ca3(PO4)2沉淀,过滤后得到2.5L滤液,测得pH为12。计算:
(1)Ca3(PO4)2(已知式量310)沉淀的质量____________;
(2)滤液中溶质的物质的量浓度__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中除铁时还常用NaClO3作氧化剂,在较小的pH条件下最终生成一种浅黄色的黄铁矾钠 [Na2Fe6(SO4)4(OH)12]沉淀除去。下图是温度-pH与生成的沉淀关系图,图中阴影部分是黄铁矾稳定存在的区域。下列说法不正确的是 {已知25℃,Ksp[Fe(OH)3]=2.64×10-39}
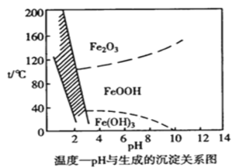
A.工业生产黄铁矾钠,温度控制在85~95℃pH=1.5左右
B.pH=6,温度从80℃升高至150℃体系得到的沉淀被氧化
C.用氯酸钠在酸性条件下氧化Fe2+ 离子方程式为:6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O
D.在25℃时溶液经氧化,调节溶液pH=4 ,此时溶液中c(Fe3+)=2.64×10-9 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(n代表能层序数)( )
A.L电子层不包含d能级
B.s电子绕核旋转,其轨道为一个圆,而p电子是走“∞”形
C.当![]() 时,该能层不一定有四个原子轨道
时,该能层不一定有四个原子轨道
D.当![]() 时,该能层有3s、3p、3d、3f四个原子轨道
时,该能层有3s、3p、3d、3f四个原子轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X与Y可形成化合物![]() ,Z元素可形成负一价离子。下列说法正确的是( )
,Z元素可形成负一价离子。下列说法正确的是( )
A.X元素原子的基态电子排布式为![]()
B.X元素是第四周期第ⅤA族元素
C.Y元素原子的电子排布图为![]()
D.Z元素的单质![]() 在氧气中不能燃烧
在氧气中不能燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2NO2(g)![]() N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
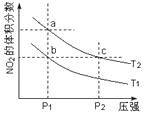
A.a、c两点气体的颜色:a浅,c深
B.a、c两点气体的平均相对分子质量:a>c
C.b、c两点的平衡常数:Kb=Kc
D.状态a通过升高温度可变成状态b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘酸钾作为食盐—碘添加剂,而碘化钾则是化工生产中一种重要原料。还原法生产碘化钾是由碘与氢氧化钾反应生成碘酸钾后,用甲酸还原而得,其主要流程如图。
请回答下列问题:
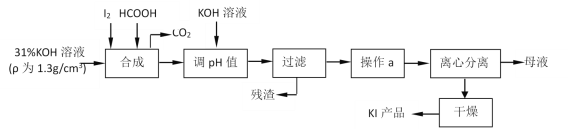
(1)判断“合成”过程中,碘是否已完全反应的方法是___。
(2)实验室中,过滤操作要求“一贴二低三靠”,其中“三靠”是指盛有被过滤液体的烧杯注液口紧靠玻璃棒、___、___。
操作a包括“蒸发浓缩、冷却结晶”是依据KI具有何种性质:___。
(3)写出“合成”过程中,HCOOH参与的离子反应方程式:___。
(4)测定产品中KI含量的方法是:
a.称取3.340g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL溶液于锥形瓶中,加入足量KIO3,用少量稀硫酸酸化所,使KIO3与KI反应完全;
c.以淀粉为指示剂,用0.2400mol/L的Na2S2O3溶液滴定,消耗溶液体积平均值为10.00mL。
已知:IO3-+I-+H+→I2+H2O(未配平),I2+2S2O32-→2I-+S4O62-。
①测定过程所需仪器在使用前必须检查是否漏液的有___。
②该样品中KI的质量分数为___。(保留3位有效数字)
(5)有学生选用家庭厨房中的有关调料(如黄酒、白醋、酱油、味精等),用简便方法来检测是否是加碘食盐。通过实践,发现厂商只要在食盐包装的封口处夹一条碘化钾淀粉试纸,并在袋上注明使用方法就能鉴别真伪。现请你写出检测使用说明书___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 有机物Y是一种治疗心血管和高血压的药物,某研究小组以甲苯、乙烯等物质为主要原料,通过以下路线合成:
有机物Y是一种治疗心血管和高血压的药物,某研究小组以甲苯、乙烯等物质为主要原料,通过以下路线合成:

已知:RX+NaCN![]() RCN
RCN![]() RCOOH
RCOOH

请回答:
(1)Y的化学式为______________
(2)写出化合物H的结构简式_______________。
(3)下列说法不正确的是______________。
A.B的一氯代物有三种
B.反应①②③④均属于取代反应
C.化合物G→Y的转化过程中,涉及的反应类型有取代反应、加成反应
D.反应①的试剂与条件为Cl2/光照
E. 化合物E能发生银镜反应
(4)写出反应④的化学方程式________________。
(5)芳香族化合物M是B的同分异构体,M含有二个六元环(且两个二元环共用两个相邻的碳原子),则M可能的结构有_______________。(任写两种)
(6)已知一个碳原子上连有两个羟基是不稳定的,会脱水转化为羰基。:![]() .写出以
.写出以![]() 为原料制备合成
为原料制备合成 的线路图。___________
的线路图。___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com