
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。某校课外兴趣小组以两条途径分别对X进行如下实验探究,下列有关说法不正确的是
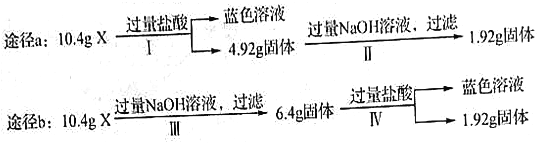
A. 由图可知X中可能存在Fe2O3 B. 可以判断混合物中是否含有Al2O3
C. 1.92g固体成分为Cu D. 依图可以计算Fe2O3和Cu的质量
【答案】A
【解析】A.取混合物10.4g,向其中加入过量的HCl,得到的溶液显蓝色,说明溶液中含有CuCl2,原固体中有Cu,由于Cu在金属活动性顺序表中排在H的后边,所以不能与酸发生反应,金属氧化物会发生反应,产生的盐与Cu发生反应,反应方程式是:Fe2O3+6HCl=2FeCl3+3H2O,然后发生反应:2FeCl3+Cu=2FeCl2+CuCl2,一定存在氧化铁,A错误;B.4.92g固体中加入过量NaOH溶液后还有剩余固体质量是1,92g,说明该固体是Cu,因此二氧化硅的质量是3g;在原固体中Fe2O3不足量,不能使Cu全部被Fe3+氧化为Cu2+;含有SiO2质量是3g;由于NaOH溶液可以与Al2O3、SiO2反应,实际溶解的质量是4.0g>3.0g,说明含有Al2O3;B正确;C.根据以上分析可知C正确;D.在10.4g固体中含有SiO23g;含有Al2O3的质量是4g-3g=1g;在加入酸溶解的质量(10.4—4.92)g=5.48g中,含有Al2O31g;则其余4.48g是Fe2O3和Cu,根据方程式Fe2O3+6HCl=2FeCl3+3H2O,2FeCl3+Cu=2FeCl2+CuCl2可得关系式:Fe2O3~Cu。160g Fe2O3对应64gCu,现在溶解质量是4.48g,因此含有Fe2O3的质量是3.2g,含有Cu的质量是1.28g,D正确。答案选A。


科目:高中化学 来源: 题型:
【题目】下列坐标图均涉及到平衡原理,其中相关( )
A. 如图表示室温下,用0.1mol?L﹣1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3?H2O),虚线表示c(NH
如图表示室温下,用0.1mol?L﹣1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3?H2O),虚线表示c(NH ![]() ),处于M点时溶液呈中性
),处于M点时溶液呈中性
B. 如图表示2SO2(g)+O2(g)?2SO3(g)△H<0,正逆反应的平衡常数随温度的变化
如图表示2SO2(g)+O2(g)?2SO3(g)△H<0,正逆反应的平衡常数随温度的变化
C. 如图表示反应2NH3(g)?3H2(g)+N2(g),在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
如图表示反应2NH3(g)?3H2(g)+N2(g),在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D. 如图表示AgCl(s)?Ag+(aq)+Cl﹣(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
如图表示AgCl(s)?Ag+(aq)+Cl﹣(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)完成下列反应的化学方程式:
①SO2通入H2O2溶液中:___________________________。
②实验室制SO2: __________________________。
③实验室制氨气:__________________________。
④足量的铁粉溶于稀硝酸:________________________。
(2)为了验证木炭和浓H2SO4反应生成的CO2、SO2,选用下图所示仪器(内含物质)组装成实验装置:

①如按气流由左向右流向,连接上述装置的正确顺序是(填接口名称):__________。
②有怎样的实验现象才表明已检验出CO2?___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系见图,下列说法正确的是( ) 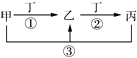
A.若丁为用量最大,用途最广的金属单质,乙的溶液一定为FeCl3
B.若通常情况下甲、乙、丙、丁都是气体,且乙和丁为空气的主要成分,则反应①的化学方程式为4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
C.若甲、乙、丙的溶液显碱性,则丙可能可以作为医疗上治疗胃酸过多症的药剂
D.若丁为化合物,且为氯碱工业的重要产品,则甲一定为含Al3+的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知有1H216O、2H2S、3H218O、3H2S、S16O2,这些分子中含有____种核素。画出18O2-的离子结构示意图:__________。
(2)下列过程中,共价键被破坏的是________。能表示反应物的总能量高于生成物总能量的化学反应是___________。
①碘升华 ②氢气在氧气中燃烧 ③HCl 气体溶于水 ④酒精溶于水
⑤冰融化 ⑥氢氧化钠熔化 ⑦NH4Cl受热分解 ⑧(NH4)2SO4溶于水
(3)根据元素周期表和元素周期律分析下面的推断,其中错误的是_______。
①砹(At)的氢化物不稳定 ②硒(Se)化氢比硫化氢稳定
③铍的原子失电了能力比镁弱 ④氢氧化铝比氢氧化钙的碱性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室制备乙酸正丁酯的化学方程式为:CH3COOH+CH3CH2CH2CH20H ![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
制备过程中还可能有的副反应有
2CH3CH2CH2CH2OH ![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O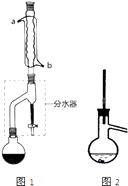
主要实验步骤如下:
Ⅰ合成:
在干燥的圆底烧瓶中加11.5mL(9.3g,0.125mol)正丁醇、7.2mL(7.5g,0.125mol)冰醋酸和3~4滴浓H2SO4 , 摇匀后,加几粒沸石,再按图1示装置安装好.在分水器中预先加入5.00mL水,其水面低于分水器回流支管下沿3~5mm,然后用小火加热,反应大约40min.
Ⅱ分离与提纯:
①将烧瓶中反应后的混后物冷却后与分水器中的酯层合并,转入分液漏斗,依次用10mL水,10mL 10%碳酸钠溶液洗至无酸性(pH=7),充分振荡后静置,分去水层.
②将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥.
③将乙酸正丁酯粗产品转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品.主要试剂及产物的物理常数如下:
化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
密度/gmL﹣1 | 0.810 | 1.049 | 0.882 | 0.7689 |
沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
根据以上信息回答下列问题:
(1)如图1整个装置可看作由分水器、圆底烧瓶和(填仪器名称)组成,其中冷水应从(填a或b)管口通入.
(2)如何判断该合成反应达到了终点: .
(3)在操作步骤①时,用右手压住分液漏斗的玻璃塞,左手握住将分液漏斗倒转过来,用力振荡,振摇几次后要放气,放气时支管口不能对着人和火.在操作步骤②后(即酯层用无水硫酸镁干燥后),应先(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中.
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在中加热比较合适(请从下列选项中选择).A.水 B.甘油(沸点290℃) C.砂子 D.石蜡油(沸点200~300℃)
如果蒸馏装置如图2所示,则收集到的产品中可能混有杂质.
(5)反应结束后,若放出的水为6.98mL(水的密度为1gmL﹣1),则正丁醇的转化率约为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D都是中学化学中常见的有机化合物,它们在一定的条件下有如下转化关系(部分物质和条件被略去).其中,A是最简单的烯烃,分子式为C2H4 , 其产量可用来衡量一个国家石油化工发展的水平.C是生活中常用的一种具有酸味的调味品的成分;通常状况下,D是具有浓郁香味的油状液体. 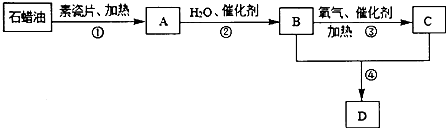
(1)在有机化合物A,B,C,D中,属于烃类的是(填结构简式);反应④的反应类型是 .
(2)在A,B,C,D中,密度比水小且难溶于水的液体是(填物质名称).A在一定条件下可以发生加聚反应生成一种塑料,该塑料的结构简式为 .
(3)反应①中,素瓷片的主要作用是 . 一定条件下, B,C,D三种物质中不能和NaOH溶液反应发生反应的是(填物质名称).
(4)植物秸秆在一定条件下能水解成葡萄糖,葡萄糖在酒化酶的作用下能转化为B,B在某种微生物存在下发生氧化反应得到C.写出葡萄糖转化为B的化学方程式: .
(5)在实验室获得的D中往往含有少量的B,C;为提纯D,可以先将此不纯的D和一充分混合,然后再静置、(填操作名称)即可.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com