
【题目】现有下列5 种物质:①空气 ②CO2 ③乙醇 ④CaCO3 ⑤Al(OH)3;按要求填空(填代号):
(1)属于混合物的是_______;
(2)属于氧化物的是_______;
(3)属于碱的是_______;
(4)属于有机物的是_______;
(5)属于盐的是_______。
科目:高中化学 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,五种元素核内质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)A2W的电子式为________。
(2)B中质子数和中子数相等的核素符号为____,E元素在周期表中的位置为_______ 。
(3)W、D、E三种元素的简单离子半径由小到大的顺序为_______(填离子符号)。
(4)在一定条件下,D元素的单质能与A元素的单质化合生成DA,DA能与水反应放氢气,则其化学方程式为_______,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是______L(标准状况下)。
(5)若要比较D和E的金属性强弱,下列实验方法可行的是_______。
a.将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱
b.将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强
C.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的原子核外M层上有3个电子,元素Y形成的离子Y2-核外有18个电子,则这两种元素可形成化合物( )
A.XY2B.X2Y3C.X3Y2D.X2Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料的不断发展可以促进社会的进步,性能各异的各种材料的广泛应用大大提高了人们的生活水平。回答下列问题:
(1)橡胶是制造轮胎的重要原料,天然橡胶通过硫化处理,使它的分子转化为体型结构,从而增大橡胶的强度,橡胶属于____(填字母)。
a. 无机非金属材料 b. 金属材料 c. 有机高分子材料
保持洁净安全的生存环境已成为全人类的共识。
(2)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行__________________ 。对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为 ___________________________________________ 。
(3)获得洁净安全的饮用水是每个人的正常需要。某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉或漂白精片进行杀菌消毒,其原理可用化学方程式表示为______________________________ 。
(4)天然水中含有细小悬浮颗粒或胶体颗粒,可以用 ____ (填一种物质的化学式)作为混凝剂净化处理。明矾净水工作原理的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯(CH3OCOOCH3,简称DMC),是一种无毒、用途广泛的化工原料,被誉为当今有机合成的“新基石”。
(1)浙江大学用甲醇、CO、O2在常压、70~120℃和催化剂的条件下合成DMC的研究开发。已知:
(ⅰ)CO的标准燃烧热:283.0 kJmol﹣1,
(ⅱ)1mol H2O(l)完全蒸发变成H2O(g)需吸收44kJ的热量
(ⅲ)2CH3OH(g)+CO2(g) ![]() CH3OCOOCH3(g)+H2O(g) △H=﹣15.5kJmol﹣1
CH3OCOOCH3(g)+H2O(g) △H=﹣15.5kJmol﹣1
则2CH3OH(g)+CO(g)+1/2O2(g) ![]() CH3OCOOCH3(g)+ H2O(l) △H=______.
CH3OCOOCH3(g)+ H2O(l) △H=______.
该反应在常压和70~120℃条件下就能自发反应的原因是___________________.
(2)甲醇和CO2可直接合成DMC:
2CH3OH(g)+CO2(g) ![]() CH3OCOOCH3(g)+H2O(g),但由于甲醇转化率通常不会超过1%,因此制约该反应走向工业化生产.
CH3OCOOCH3(g)+H2O(g),但由于甲醇转化率通常不会超过1%,因此制约该反应走向工业化生产.
①写出该反应平衡常数表达式:______________________________.
②在恒容密闭容器中发生上述反应,能说明已达到平衡状态的是__________(选填编号)。
A.v正(CH3OH)=2v逆(CO2) B.CH3OCOOCH3与H2O的物质的量之比保持不变
C.容器内气体的密度不变 D.容器内压强不变

③某研究小组在某温度下,在100mL恒容密闭容器中投入2.5mol CH3OH(g)、适量CO2和6×10﹣5 mol催化剂,研究反应时间对甲醇转化数(TON)的影响,其变化曲线如图所示。(计算公式:TON=转化的甲醇的物质的量/催化剂的物质的量)在该温度下,最佳反应时间是_____;4~10h内DMC的平均反应速率是_______.
④如果在其它条件不变的情况下,研究反应温度对甲醇转化数(TON)的影响,请在图的坐标系中画出从投入反应物开始,随着反应温度不断升高(不考虑温度对催化剂活性的影响),TON变化的曲线示意图(假设起始温度为T0℃)__________________.

⑤假设在密闭容器中发生上述反应,达到平衡时下列措施能提高TON值的是______.
A.往反应体系中添加催化剂 B.往反应体系中添加吸水剂
C.从反应体系中分离出CO2 D.扩大容器的体积.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米技术”广泛应用于催化及军事科学中,“纳米材料”是粒子直径在1~100 nm(纳米)之间的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③是浊液 ④不能透过滤纸
⑤能透过滤纸 ⑥能产生丁达尔效应 ⑦静置后,会析出黑色沉淀
A. ②⑤⑥ B. ②⑥⑦ C. ①⑤ D. ③④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)制备精细化工产品PbSO4·3PbO·H2O(三盐)的主要流程如下:

已知:常温下,Ksp(PbSO4)=2.0×10-8 Ksp(PbCO3)=1.0×10-13 ,请回答以下问题:
(1)铅蓄电池工作原理是PbO2+Pb+2H2SO4![]() 2PbSO4+2H2O,在放电过程中负极的质量__________;电解质溶液的pH___________(用“变大”、“不变”或“变小”填写)。该铅蓄电池放电过程中的正极反应式为__________________________________________。
2PbSO4+2H2O,在放电过程中负极的质量__________;电解质溶液的pH___________(用“变大”、“不变”或“变小”填写)。该铅蓄电池放电过程中的正极反应式为__________________________________________。
(2)步骤③的目的是使铅泥中的Pb溶解,其对应的离子方程式为________________ 。滤液2中的溶质主要是_____________(填化学式),过滤操作中使用到的玻璃仪器有_____。
(3)步骤⑥合成三盐的化学方程式为________________________。
(4)步骤⑦洗涤产品的方法是________________________________。
(5)在“转化”过程中,若PbSO4和PbCO3在悬浊液中共存,则c(SO42-):c(CO32-)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品,试根据下图回答有关问题:
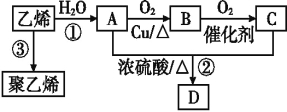
已知:有机物D是一种有水果香味的油状液体。
(1)有机物B的名称为 ,结构简式为 。
决定有机物A、C的化学特性的原子团的名称分别是 。
(2)写出图示反应②、③的化学方程式,并指明反应类型:
② ; 反应类型: 。
③ ; 反应类型: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com