
 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图所示:
| ||
| ||
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某有机物的结构式如图它在一定条件下可能发生的反应有①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥加聚( )
某有机物的结构式如图它在一定条件下可能发生的反应有①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥加聚( )| A、②③④ | B、①③⑤⑥ |
| C、①③④⑤ | D、②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ①图象中曲线
①图象中曲线| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40[ |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
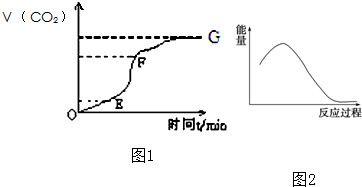
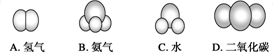
查看答案和解析>>
科目:高中化学 来源: 题型:
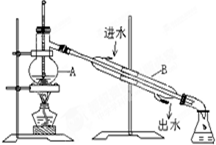 图中装置中仪器的名称:
图中装置中仪器的名称:查看答案和解析>>
科目:高中化学 来源: 题型:
 有一反应,由X与Y化合生成Z.其反应如右:2X+3Y=2Z,反应物X与生成物Z的质量关系如图.下列说法正确的是( )
有一反应,由X与Y化合生成Z.其反应如右:2X+3Y=2Z,反应物X与生成物Z的质量关系如图.下列说法正确的是( )| A、有4g的Z生成时,则消耗Y 6g |
| B、X、Y、Z的摩尔质量之比为3:2:6 |
| C、2mol X质量与3mol Y质量之和等于2mol Z的质量 |
| D、消耗2mol X时,在标准状况下,生成Z的体积为44.8L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于非金属性Y>R,则X、Y组成化合物的稳定性高于X、R组成的化合物 |
| B、在Z、Y形成的两种离子化台物中阴阳离子的个数比分别均为1:2 |
| C、原子半径由大到小排列的顺序是:Z>R>W>Y>X |
| D、Y、Z、W三种元素组成化合物的水溶液一定显碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com