
【题目】设阿伏加德罗常数为NA,下列说法不正确的是( )
A.常温常压下,30 g乙烷气体中所含有的共价键数目为6NA
B.含1 mol Cl-的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中NH4+数为NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为l.5NA
D.在电解精炼铜的过程中,当阴极析出32g铜单质时,电子转移数目为NA
【答案】A
【解析】
A.常温常压下,乙烷分子的结构简式为CH3CH3,一个乙烷分子中含有7个共价键,30g乙烷气体中所含有的共价键数目为![]() ×NA=7NA,故A错误;
×NA=7NA,故A错误;
B.溶液存在c(NH4+)+c(H+)=c(Clˉ)+c(OHˉ),溶液呈中性,则氢氧根离子浓度等于氢离子浓度,氨根离子浓度等于氯离子浓度,氨根离子的物质的量等于氯离子的物质的量,Cl-的物质的量为1 mol,则NH4+的物质的量为1mol,NH4+数为NA,故B正确;
C.乙烯和丁烯的最简式为CH2,21.0g乙烯和丁烯的混合气体含有CH2的物质的量n=![]() ,一个CH2基团中含有一个碳原子,含有的碳原子数目为l.5NA,故C正确;
,一个CH2基团中含有一个碳原子,含有的碳原子数目为l.5NA,故C正确;
D.32g铜的物质的量为![]() ,而生成1mol铜时转移2mol电子,故当生成0.5mol铜时转移1mol电子,电子的数目为NA个,故D正确;
,而生成1mol铜时转移2mol电子,故当生成0.5mol铜时转移1mol电子,电子的数目为NA个,故D正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】有关水的电离平衡的说法正确的是( )
A.水的离子积通常用![]() 来表示,只适用于纯水,在稀盐酸中数值会变大
来表示,只适用于纯水,在稀盐酸中数值会变大
B.在纯水中加入硫酸会抑制水的电离,加醋酸会促进水的电离
C.盐溶于水对水的电离平衡均没有影响,水溶液一定呈中性
D.在纯水中加入氢氧化铁固体对水的电离平衡会有微弱的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备苯甲醇和苯甲酸的化学原理是
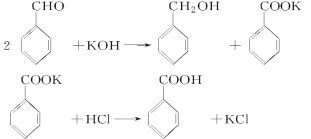
已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3 ℃;苯甲酸的熔点为121.7 ℃,沸点为249 ℃,溶解度为0.34 g;乙醚的沸点为34.8 ℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:
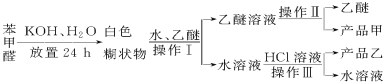
试根据上述信息回答下列问题:
(1)操作Ⅰ的名称是________,乙醚溶液中所溶解的主要成分是________。
(2)操作Ⅱ的名称是________,产品甲是________。
(3)操作Ⅲ的名称是________,产品乙是________。
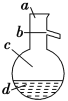
(4)如图所示,操作Ⅱ中温度计水银球上沿放置的位置应是________(填“a”“b”“c”或“d”),该操作中,除需蒸馏烧瓶、温度计外,还需要的玻璃仪器是__________________,收集产品甲的适宜温度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:
(1)2A(g) ![]() 2B(g)+C(g); (2)A(g)
2B(g)+C(g); (2)A(g) ![]() C(g)+D(g)。
C(g)+D(g)。
当达到平衡时,测得c(A)=2.5 mol·L-1(表示该物质浓度,下同),c(C)=2.0 mol·L-1。则下列说法中正确的是( )
A.达到平衡时A的总转化率为40%B.达到平衡时c(B)为1.0 mol·L-1
C.达到平衡时c(B)=2c(D)D.达到平衡时c(D)=2c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于酸碱中和滴定实验的说法正确的是( )

A.用图B的滴定管可准确量取25.00mL的酸性KMnO4溶液
B.滴定过程中,眼睛要时刻注视滴定管中液面的变化
C.滴定管装入液体前需用待装液润洗
D.滴定前平视,滴定结束后仰视读数,不影响测定结果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在10 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液20 mL,溶液中含碳微粒的物质的量随溶液pH的变化如图所示。下列说法错误的是( )
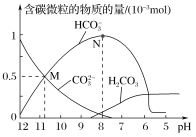
A.HCl溶液滴加一半时,溶液pH>7
B.H2CO3的Ka1的数量级为10-6
C.pH=8时,溶液中NaHCO3的物质的量浓度为0.1 mol·L-1
D.在M点:c(Na+)>c(CO![]() )=c(HCO
)=c(HCO![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是人类利用最早的金属之一,其单质及化合物在人生产生活中有着广泛的应用。
(1)铜可以做成导线,Cu的焰色为___________色;基态Cu2+的核外电子占据的最高能层的能层符号为___________。
(2)铜可以作为乙醇和氧气反应的催化剂,2CH3CH2OH + O2![]() CH3CHO + 2H2O。写出与水具有相同空间构型的一个分子和一个离子______________(微粒由短周期元素组成)。从原子轨道重叠方式来看CH3CHO中所含的共价键类型有____________________,碳的杂化方式是______________。
CH3CHO + 2H2O。写出与水具有相同空间构型的一个分子和一个离子______________(微粒由短周期元素组成)。从原子轨道重叠方式来看CH3CHO中所含的共价键类型有____________________,碳的杂化方式是______________。
(3)高温超导是世界上最前沿的研究之一,如下图是第一个被发现的高温超导体氧化物的晶胞。该化合物的化学式为___________。与Cu2+紧邻的O2-的个数为___________。已知,阿伏加德罗常数为NA,则晶胞密度为___________g·cm-3。
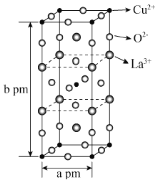
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年11月4日是《巴黎协定》气候协议生效的日期,其宗旨是提高绿色低碳转型的竞争力、抵御气候变化,人们需要用不同的方法将CO2进行转化利用。
(1)处理CO2的方法之一是使其与氢气反应合成甲醇。已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(1) △H=-283.0kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(1) △H=-726.0kJ·mol-1
写出二氧化碳与氢气合成甲醇液体的热化学方程式_________;
(2)CO2经催化加氢还可合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) △H=QkJ·mol-1在0.1MPa时,按n(CO2):n(H2)=1:3投料,右图表示平衡时四种气态物质的物质的量(n)与温度(T)的关系。
C2H4(g)+4H2O(g) △H=QkJ·mol-1在0.1MPa时,按n(CO2):n(H2)=1:3投料,右图表示平衡时四种气态物质的物质的量(n)与温度(T)的关系。
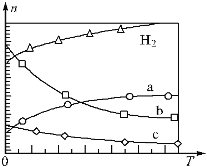
①Q______0(填“>”、“=”或“<”);
②曲线b表示的物质为_____。
(3)在强酸性的电解质水溶液中,用惰性材料做电极,电解CO2可得到多种燃料,其原理如右图所示。

①该工艺中能量转化方式主要有______;
②电解时,生成丙烯(C3H6)的电极反应式为______。
(4)以CO2为原料制取碳(C)的太阳能工艺如右图所示。

①过程1中发生反应的化学方程式为______;
②过程2中每生成1molFe3O4[FeOFe2O3]转移电子的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是 ( )
A. 稀硫酸滴在铁片上:2Fe+6H+===2Fe3++3H2↑
B. 碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=H2O+CO2↑
C. 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-===Cu(OH)2↓+![]()
D. 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-===AgCl↓+![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com