
| ||
| 5-2 |
| ||
| 5-2 |


科目:高中化学 来源: 题型:
| A、F2与NaOH溶液反应:F2+4OH-=2F-+O2+2H2O |
| B、等体积等浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2=Fe3++2H2O |
| D、淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O=2I2+4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液呈碱性,c(CH3COO-)<c(Ba2+) |
| B、c(Ba2+)+c(H+)=2c(CH3COO-)+c(OH-) |
| C、c(Ba2+)=c(CH3COO-)+c(CH3COOH) |
| D、加入少量Ba(OH)2固体,溶液中c(CH3COO-)和c(Ba2+)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
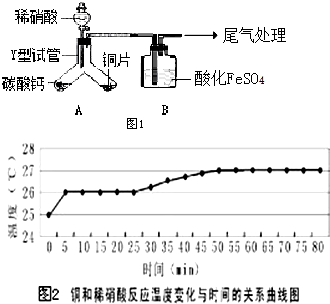 为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验.
为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验.| 间/min | 现象 |
| 0~15 | 铜表面出现气泡,但速度很慢 |
| 25 | 溶液有很浅的蓝色,气泡生成速度加快 |
| 30 | 气泡生成速度较快,均匀冒出 |
| 45 | 洗气瓶中可见少量淡棕色的物质 |
| 50 | 溶液中蓝色明显变深,洗气瓶中突显明显棕色 |
| 序号 | 温度 | 铜片/g | 硝酸/mL | 硝酸铜/g |
| 1 | 25℃ | ① | ② | ③ |
| 2 | 25℃ | 5 | 20 | 0.5 |
| 3 | 25℃ | 5 | 20 | 1.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
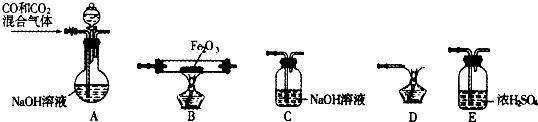
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com