
【题目】用化学用语表示CH4+Cl2![]() CH3Cl+HCl中的相关微粒,其中错误的是
CH3Cl+HCl中的相关微粒,其中错误的是
A. 中子数为20的氯原子:![]()
B. Cl的结构示意图:![]()
C. CH4的比例模型: ![]()
D. HCl的电子式:H∶Cl
【答案】D
【解析】
A.质量数=质子数+中子数,元素符号的左上角为质量数;
B、氯原子是17号元素,核外最外层电子数为7。
C、甲烷是碳原子和氢原子间通过共价单键形成的空间正四面体结构;
D、氯化氢为共价化合物,分子中含有1个H-Cl键,氯原子最外层电子未标注;
A.质子数为17、中子数为20的氯原子的质量数=17+20=37,该原子正确的表示方法为:1737Cl,故A正确;
B、氯原子是17号元素,核外电子分为三个电子层,原子结构示意图为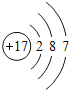 ,故B正确;
,故B正确;
C、甲烷是碳原子和氢原子间通过共价单键形成的空间正四面体结构,CH4的比例模型: ![]() ,故C正确;
,故C正确;
D、HCl为共价化合物,电子式中需要标出最外层电子,氯化氢正确的电子式为![]() ,故D错误;
,故D错误;
故选D。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16,三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子。有关判断不正确的是
( )
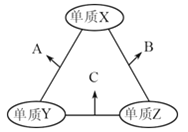
A. A不能溶解于B中
B. X元素位于ⅥA族
C. B的沸点高于C的沸点
D. A和C不可能发生氧化还原反应,X与Y能形成两种化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2HI(g) == H2(g) + I2(g)的ΔH= +11 kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为
A.576 kJB.283 kJC.598 kJ·D.299 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应:I2(g)+H2(g)![]() 2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
编号 | 改变的条件 | 反应速率 |
(1) | 升高温度 | ______ |
(2) | 加入正催化剂 | ______ |
(3) | 再充入a mol H2 | ______ |
(4) | 将容器的容积扩大到原来的2倍 | ______ |
(5) | 保持容积不变,通入b mol Ne | ______ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物吗替麦考酚酯有强大的抑制淋巴细胞增殖的作用,可通过如下反应制得:
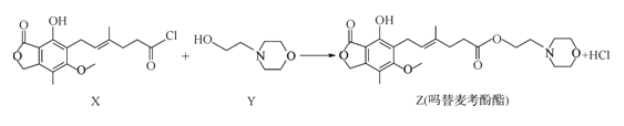
下列叙述正确的是
A. 化合物X的分子式为C17H18O5Cl
B. 化合物Y的属于α—氨基酸的同分异构体数目为4种
C. 1 mol化合物Z可以与4 mol NaOH反应
D. 用FeCl3溶液可鉴别化合物X和Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如下实验(夹持装置未画出)进行实验。请回答下列问题:
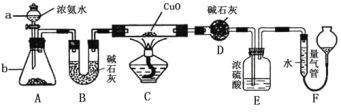
(1)仪器a的名称为____________;仪器b中可选择的试剂为(任意填一种)_____________。
(2)实验中,装置C中黑色CuO粉末全部转化为红色固体(已知Cu2O也为红色固体),量气管中有无色无味的气体。实验前称取黑色CuO 80g,实验后得到红色固体质量为68g。则红色固体成分的化学式为_______________。
(3)E装置中浓硫酸的作用是____________________________________。
(4)F中读取气体体积前,应对装置F进行的操作是:___________________,若无此操作,而F中左边液面低于右边液面,会导致读取的气体体积________ (填“偏大”或“偏小”或“无影响”);图中量气管可由________ (请选择字母填空:A.酸式滴定管,B.碱式滴定管)改装而成。
(5)要想测得氨气分子中氮、氢原子个数比,实验中应至少测量或读取哪些数据________。
A.B装置实验前后质量差mg; B.F装置实验前后液面差VL
C.D装置实验前后质量差mg; D.E装置实验前后质量差mg;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液里大量共存的是( )
A.无色溶液: H+、NH4+、SO42-、Cr2O72-
B.Fe2+、Na+、Cl-、NO3-
C.K+、Fe3+、SCN-、SO42-
D.Na+、Al3+、HCO3一、Cl一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA是阿伏加德罗常数的值,下列说法正确的是
A. 常温常压下,6.4g O2和O3的混合气体中含有的分子数为0.4 NA
B. 标准状况下,2.24 L CCl4分子中共价键的数目为0.4NA
C. 25℃时,pH=13的Ba(OH)2溶液中含有氢氧根离子数为0.1 NA
D. 高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在相应的条件下可能大量共存的是( )
A. 能使pH试纸变红的溶液中:CO32—、K+、Cl-、Na+
B. 由水电离产生的c(OH-)=1×10-10mol·L-1的溶液中:NO3—、Mg2+、Na+、SO42—
C. 在![]() =1×1012的溶液中:NH4+、Fe2+、Cl-、NO3—
=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3—
D. ![]() =10-14mol·L-1的溶液中:Na+、HCO3—、Cl-、K+
=10-14mol·L-1的溶液中:Na+、HCO3—、Cl-、K+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com