
【题目】某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如下实验(夹持装置未画出)进行实验。请回答下列问题:
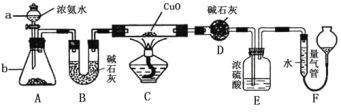
(1)仪器a的名称为____________;仪器b中可选择的试剂为(任意填一种)_____________。
(2)实验中,装置C中黑色CuO粉末全部转化为红色固体(已知Cu2O也为红色固体),量气管中有无色无味的气体。实验前称取黑色CuO 80g,实验后得到红色固体质量为68g。则红色固体成分的化学式为_______________。
(3)E装置中浓硫酸的作用是____________________________________。
(4)F中读取气体体积前,应对装置F进行的操作是:___________________,若无此操作,而F中左边液面低于右边液面,会导致读取的气体体积________ (填“偏大”或“偏小”或“无影响”);图中量气管可由________ (请选择字母填空:A.酸式滴定管,B.碱式滴定管)改装而成。
(5)要想测得氨气分子中氮、氢原子个数比,实验中应至少测量或读取哪些数据________。
A.B装置实验前后质量差mg; B.F装置实验前后液面差VL
C.D装置实验前后质量差mg; D.E装置实验前后质量差mg;
【答案】(1)分液漏斗(1分) 碱石灰或生石灰或氢氧化钠固体(任意填一种)(2分)
(2)Cu和Cu2O(3分)
(3)防止F中水蒸气进入D中,并吸收氨气(2分)
(4)向上或向下移动右管,使得左右两边液面相平(2分),偏小(2分),B(1分)
(5)B、C(2分)
【解析】
试题(1)a是分液漏斗,A是制氨气的装置,所以b中可放碱石灰或生石灰或氢氧化钠固体任意一种
(2)若CuO全部被还原为Cu,则CuO∽Cu,计算出Cu的质量为64g,但红色固体的质量为68g>64g,所以该红色固体的成分是Cu和Cu2O
(3)浓硫酸的作用是吸收未反应的氨气及防止F中的水进入D中,影响结果
(4)F中读取气体体积时应保证气体和外界大气压相等,所以应向上或向下移动右管,使得左右两边液面相平,若F中左边液面低于右边液面,说明气体压强大于外界大气压强,压强增大体积偏小,根据酸式滴定管与碱式滴定管的不同,图中量器管可由碱式滴定管改装而成,选B
(5)确定氨气分子中氮、氢原子个数比也即确定产物中水和氮气的物质的量,A、B装置是干燥氨气,其质量与所求无关,错误;B、F装置测量氮气的体积,正确;C、D装置测量产物水的质量,正确;D、E装置是吸收多余的氨气及防治水进入D中,与所求无关,所以答案选B、C


科目:高中化学 来源: 题型:
【题目】化合物乙是一种治疗神经类疾病的药物,可由化合物甲经多步反应得到。下列有关甲、乙的说法不正确的是
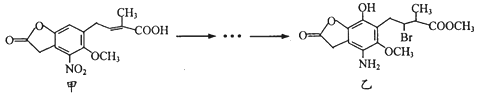
A. 甲的分子式为C14H11NO7
B. 甲和乙所含官能团均为5种
C. 可用NaHCO3溶液鉴别化合物甲和乙
D. 甲能与酸性高锰酸钾溶液反应,乙能与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电极反应的说法正确的是
A.原电池正极和电解池阳极发生还原反应B.原电池正极和电解池阴极发生氧化反应
C.原电池负极和电解池阳极发生氧化反应D.原电池负极和电解池阴极发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学用语表示CH4+Cl2![]() CH3Cl+HCl中的相关微粒,其中错误的是
CH3Cl+HCl中的相关微粒,其中错误的是
A. 中子数为20的氯原子:![]()
B. Cl的结构示意图:![]()
C. CH4的比例模型: ![]()
D. HCl的电子式:H∶Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在水溶液中大量共存的是
A.Na+、Ag+、NO3-、CO32-B.Fe2+、H+、SO42-、NO3-
C.Al3+、K+、SO42-、OH-D.Na+、Mg2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若往20 mL 0.01 mol·L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示。下列有关说法不正确的是
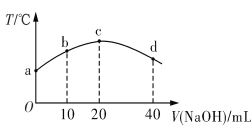
A. HNO2的电离平衡常数:c点>b点
B. b点混合溶液显酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-)
C. c点混合溶液中:c(OH-)>c(HNO2)
D. d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)铬是一种硬而脆,抗腐蚀性强的金属,常用于电镀和制造特种钢,基态Cr原子中,电子占据最高能层的符号为___,该能层上具有的原子轨道数为___。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能是否符合这一规律?___(填“是”或“否”),原因是______________(如果前一问填“是”,此问可以不答)。
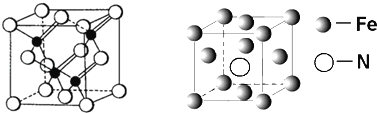
(3)镓与第VA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如下图所示(白色球代表As原子).在GaAs晶体中,每个Ga原子与____个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为_____;
(4)与As同主族的短周期元素是N、P.AsH3中心原子杂化的类型为____;一定压强下将AsH3、NH3和PH3的混合气体降温时首先液化的是_______,理由是__________;
(5)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为________;设晶胞边长为acm,阿伏加德罗常数为NA,该晶体的密度为__g.cm﹣3(用含a和NA的式子表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com