
【题目】下列措施不能加快化学反应速率的是
A.升高温度 B.降低温度
C.提高反应物浓度 D.使用合适的催化剂
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】如图是由![]() 个碳原子构成的
个碳原子构成的![]() 种有机物(氢原子没有画出):
种有机物(氢原子没有画出):
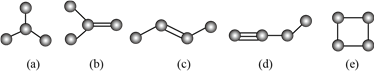
下列说法不正确的是
A. (![]() )、(
)、(![]() )、(
)、(![]() )互为同分异构体
)互为同分异构体
B. (![]() )和(
)和(![]() )的一氯代物都只有一种
)的一氯代物都只有一种
C. (![]() )和(
)和(![]() )都不能使溴在四氯化碳溶液褪色
)都不能使溴在四氯化碳溶液褪色
D. (![]() )、(
)、(![]() )、(
)、(![]() )都能使酸性高锰酸钾溶液褪色
)都能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可用于测量阿伏加德罗常数的装置示意图,其中A是纯铜片、B是石墨,插在100 mL CuSO4稀溶液中,铜片、石墨与引出导线相连,引出端分别为X、Y。
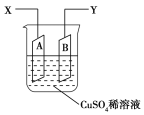
(1)当以I A的电流电解6 min后,测得铜片A质量减少2.56 g,则图装置中的X端应与直流电的________极相连。
(2)电解后将电源反接,2I A的电流电解6 min后,假设溶液体积不变,测得溶液中CuSO4物质的量浓度为0.1 mol/L,则原溶液中CuSO4物质的量浓度________mol/L。溶液中H+的物质的量浓度为________mol/L。
(3)列式计算实验测得阿伏加德罗常数NA(用I表示)________mol-1。(已知电子电量e=1.60×10-19 C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2与N2O4可相互转化:2NO2(g)![]() N2O4(g) ΔH=-24.2 kJ·mol-1,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的量浓度随时间变化的关系如下图所示。下列推理分析不合理的是( )
N2O4(g) ΔH=-24.2 kJ·mol-1,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的量浓度随时间变化的关系如下图所示。下列推理分析不合理的是( )

A. 前10 min内,用v(NO2)表示的反应速率为0.04 mol·L-1·min-1
B. 反应进行到10 min时,体系放出的热量为9.68 kJ
C. a点正反应速率小于逆反应速率
D. 25 min时,正反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或实验仪器使用正确的是
A.将高锰酸钾溶液盛装在碱式滴定管中
B.容量瓶、滴定管使用前均需用蒸馏水洗净并烘干
C.用10 mL量筒量取2.5 mL浓硫酸用于配制一定浓度的稀硫酸
D.溶液蒸发浓缩时,用坩埚钳夹持蒸发皿直接加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g) + 2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) △H2
CH3OH(g) + H2O(g) △H2
③CO2(g) + H2(g)![]() CO(g) + H2O(g) △H3
CO(g) + H2O(g) △H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O |
| H-O | C-H |
E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=_____kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=_______kJ·mol-1
(2)反应①的化学平衡常数K的表达式为_____;图1中能正确反映平衡常数K随温度变化关系的曲线为______(填曲线标记字母)。
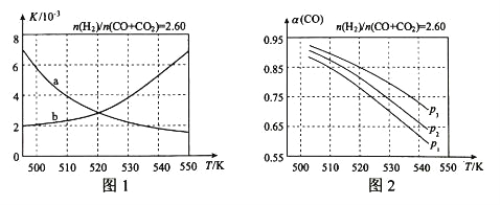
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α与温度和压强的关系如图2所示。 α(CO)值随温度升高而_______(填“增大”或“减小”)。图2中的压强由大到小为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com