
【题目】下列物质属于纯净物的是
A. 高锰酸钾完全分解后的残余物 B. 洁净的食盐水 C. 干冰 D. 白酒
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】化学小组利用如图装置进行某些气体的制备和性质实验,图中夹持装置有省略 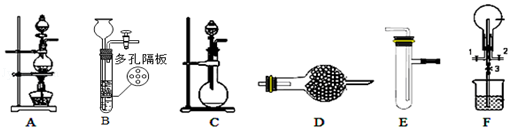
(1)为制取干燥氨气,可将装置C与装置D连接,则装置D中的固体可选用 . a.碱石灰b.无水氯化钙 c.五氧化二磷d.生石灰
(2)装置F可用于探究氯气和氨气反应,实验时打开开关1、3,关闭2,先向烧瓶中通入一种气体,然后关闭1、3,打开2,向烧瓶中缓慢通入另一种气体.实验一段时间后烧瓶内出现浓厚的白烟后在容器内壁凝结,并产生一种单质气体.写出足量氨气与氯气反应的化学方程式 . 请设计一个实验方案鉴定该固体中的阳离子 .
(3)利用装置A、E,可设计实验比较氯离子和溴离子的还原性强弱,能证明结论的实验现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液、胶体和浊液这三种分散系的根本区别是
A. 分散质粒子直径的大小 B. 是否能通过半透膜
C. 是否具有丁达尔效应 D. 是否均一、透明、稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是某研究小组探究影响反应速率部分因素的相关实验数据。
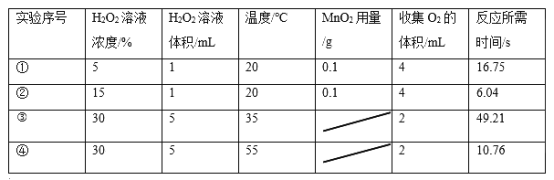
(1)写出H2O2分解的化学方程式_________________________________。
(2)通过实验①和②对比可知,化学反应速率与_________有关;从实验③和④对比可知,化学反应速率与温度的关系是_____________________________。
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总物质的量_________________(填增大、减小、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g)![]() 3C(g)+2D(g),开始时A为4 mol,B为6 mol;5 min末时测得C的物质的量为3 mol。请计算:
3C(g)+2D(g),开始时A为4 mol,B为6 mol;5 min末时测得C的物质的量为3 mol。请计算:
(1)5min末A的物质的量浓度___________________;
(2)5min内D的平均化学反应速率____________________;
(3)B的转化率_____________________________;
(4)反应后容器中的总压强与反应前总压强之比为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实际应用原理的表达式中,不正确的是
A. 用排饱和食盐水法收集Cl2: Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
B. H2燃烧热的热化学方程式:H2 (g)+1/2O2 (g) =H2O(1) △H=-285.8kJ·mol-1
C. 热的氢氟酸酸性增强:HF+H2O= H3O++F- △H>0
D. 用 TiCl4制备 TiO2:TiCl4+(x+2)H2O (过量)![]() TiO2·xH2O↓+4HCl
TiO2·xH2O↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L0.1mol·L—1的氨水中含有的NH3分子数为0.1NA
B.标准状况下,2.24L的CCl4中含有的C—Cl键数为0.4NA
C.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4 NA
D.常温常压下,Na2O2与足量CO2反应生成2.24L O2,转移电子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com