
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
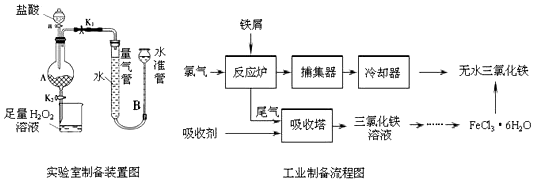
分析 (1)根据实验装置和操作步骤可知,实验室制备无水FeCl3,是利用铁与盐酸反应生成FeCl2,然后把FeCl2氧化成FeCl3,先制得FeCl3•6H2O晶体,再脱结晶水制得无水FeCl3.烧杯中足量的H2O2溶液是作氧化剂,把亚铁离子全部氧化成三价铁离子;
(2)铁与盐酸反应完全时,不再产生氢气,所以装置A中不产生气泡或量气管和水准管的液面不再变化,此时,可将A中FeCl2溶液放入烧杯中进行氧化.
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入盐酸后,蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)从工业制备流程图分析可知,反应炉中进行的反应是 2Fe+3Cl2=2FeCl3,因此,进入吸收塔中的尾气是没有参加反应的氯气,在吸收塔中氯气被吸收剂吸收,反应后生成2FeCl3溶液,所以吸收剂应是2FeCl2溶液,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-.
(5)捕集器收集的是气态FeCl3,FeCl3的相对分子质量是162.5,由相对分子质量为325的铁的氯化物可以推出,当温度超过673K时,二分子气态FeCl3可以聚合生成双聚体Fe2Cl6;
(6)①根据c(待测液)=$\frac{c(标准液)V(标准液)}{V(待测液)}$分析不当操作对相关物理量的影响,以此判断浓度的误差;
②根据2Fe3++2I -=2Fe2++I2; I2+2S2O32-═2I-+S4O62-;可得关系式:2Fe3+~I2~2S2O32-,根据Na2S2O3的物质的量求得氯化铁的质量,进而求样品中氯化铁的质量分数.
解答 解:(1)根据实验装置和操作步骤可知,实验室制备无水FeCl3,是利用铁与盐酸反应生成FeCl2,然后把FeCl2氧化成FeCl3,先制得FeCl3•6H2O晶体,再脱结晶水制得无水FeCl3.烧杯中足量的H2O2溶液是作氧化剂,把亚铁离子全部氧化成三价铁离子;
故答案为:把亚铁离子全部氧化成三价铁离子;
(2)铁与盐酸反应完全时,不再产生氢气,所以装置A中不产生气泡或量气管和水准管的液面不再变化,此时,可将A中FeCl2溶液放入烧杯中进行氧化;
故答案为:装置A中不产生气泡或量气管和水准管液面不变;
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入盐酸后,蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
故答案为:盐酸;
(4)从工业制备流程图分析可知,反应炉中进行的反应是 2Fe+3Cl2=2FeCl3,因此,进入吸收塔中的尾气是没有参加反应的氯气,在吸收塔中氯气被吸收剂吸收,反应后生成2FeCl3溶液,所以吸收剂应是2FeCl2溶液,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(5)捕集器收集的是气态FeCl3,FeCl3的相对分子质量是162.5,由相对分子质量为325的铁的氯化物可以推出,当温度超过673K时,二分子气态FeCl3可以聚合生成双聚体Fe2Cl6;
故答案为:Fe2Cl6;
(6)①A.锥形瓶未润洗,导致标准液被稀释,消耗的标准液体积偏高,则测定结果偏大,故A错误;
B.锥形瓶中溶液变色后立刻停止滴定,反应液未充分混合,进行读数标准液使用偏少,测定结果偏低,故B正确;
C.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡,则标准液体积读数偏小,测定结果偏低,故C正确;
D.滴定终点时仰视读数,读数比实际偏大,测定结果偏大,故D错误;
故答案为:BC;
②由反应:2Fe3++2I -=2Fe2++I2; I2+2S2O32-═2I-+S4O62-;可得关系式:
2Fe3+-I2-2S2O32-
1 1
n cV×10-3
所以 n(Fe3+)=c•V•10-3 mol×10=0.01cVmol,
所以m克无水氯化铁样品中氯化铁的质量为0.01cVmol×162.5g/mol=1.625cVg
所以m克无水氯化铁样品中氯化铁的质量分数为$\frac{1.625cVg}{mg}×100%$=$\frac{162.5cV}{m}$%;
故答案为:$\frac{162.5cV}{m}%$.
点评 本题考查学生对工艺流程的理解、物质的分离提纯等基本操作、氧化还原反应滴定应用、溶度积有关计算等,难度中等,需要学生具有扎实的基础知识与灵活运用知识解决问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | SO2是形成酸雨的主要气体 | |
| B. | 用碱液吸收燃煤废气可减少环境污染 | |
| C. | 用水溶解、过滤除去煤中的单质硫以减少SO2排放 | |
| D. | 往燃煤中混入生石灰,可减少SO2排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体通过盛有水的洗气瓶 | |
| B. | 通过装有过量浓溴水的洗气瓶 | |
| C. | 先将混合气体通过酸性高锰酸钾溶液中,然后再通入NaOH溶液中 | |
| D. | 混合气与过量氢气混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 34S2-的结构示意图: | B. | H2O2的电子式: | ||
| C. | 甲烷分子的比例模型: | D. | 中子数为18的硫原子:${\;}_{16}^{18}$S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
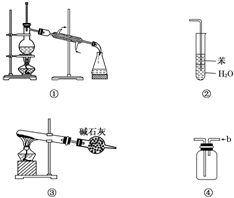
| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收氨气,能够防止倒吸 | |
| C. | 以NH4HCO3为原料,装置③可用于制备少量CO2 | |
| D. | 装置④a口进气可收集Cl2、NO2等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeSO4溶液中滴加NaOH浓液 | B. | 碳酸氢钠溶液中滴加稀盐酸溶液 | ||
| C. | 硫酸铁溶液中滴加硫氰化钾溶液 | D. | 氯化铁溶液中加入还原性铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①③④ | C. | ①③⑤⑥ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取氯气时为防止中毒应在露天的环境中进行 | |
| B. | 用试管加热碳酸氢钠固体时使试管口略向上倾斜 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 金属钠着火时应使用沙土盖灭 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com