

| ||
| ||
bg×
| ||
| ag |
| 54b |
| 102a |
| 54b |
| 102a |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、AlO2-,K+,SO42-,Cl- |
| B、K+,Br-,SO42-,Na+ |
| C、Fe3+,NO3-,Na+,S2- |
| D、I-,Cl-,Mg2+,SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠保存在无水乙醇中 |
| B、冷的浓H2SO4存放于敞口铝制容器中 |
| C、少量的白磷保存在二硫化碳中 |
| D、氯气液化后贮存于钢瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
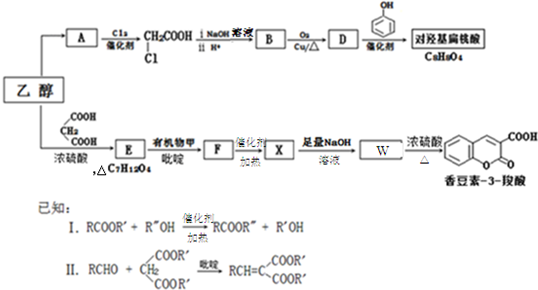
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钠能与盐酸反应,医疗上常用碳酸钠治疗胃酸过多 |
| B、铁比铜活泼,在海轮外壳上安装铜块以减缓船体腐蚀 |
| C、漂白粉在空气中不稳定,可以用来漂白纸张 |
| D、二氧化硫具有较强的还原性,故常用作葡萄酒的抗氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
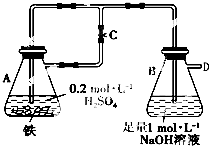 铁是人类应用较早,当前应用量最大的金属元素.
铁是人类应用较早,当前应用量最大的金属元素.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中有晶体析出,Na+数目不变 |
| B、溶液中有气体逸出,Na+数目增加 |
| C、溶质的质量分数增大 |
| D、溶液中Na+数目减少,溶质质量分数未变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | 实验结论 | 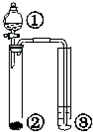 | |
| A | 稀醋酸 | CaCO3 | 澄清石灰水 | 酸性:醋酸>碳酸 | |
| B | 硫酸 | Na2SO3 | 溴水 | SO2具有还原性 | |
| C | 浓盐酸 | KMnO4 | 淀粉KI溶液 | 氧化性:KMnO4>Cl2>I2 | |
| D | 盐酸 | Na2CO3 | Na2SiO3 | 非金属性:Cl>C>Si |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、250 mL、13.6 g |
| B、500 mL、5.6 g |
| C、125 mL、10.2 g |
| D、1000 mL、7.8 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com