
【题目】下列各物质的分类、名称(或俗名)、化学式都正确的是 ( )
A. 氧化物 氧化铁 FeOB. 盐 胆矾 CuSO45H2O
C. 酸 硫酸 H2SD. 碱 纯碱 Na2CO3
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中溶质的物质的量浓度为1mol/L的是 ( )
A. 将40gNaOH溶解于1L水中配成NaOH溶液
B. 常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液
C. 将1L0.5mol/L的浓盐酸加热浓缩为V/2L
D. 从1000ml1mol/L的NaCl溶液中取出100ml的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在铁质品上镀上一定厚度的锌层,以下电镀方案正确的是( )
A.锌作阳极,铁制品作阴极,溶液中含Zn2+
B.锌作阳极,铁制品作阴极,溶液中含Fe3+
C.锌作阴极,铁制品作阳极,溶液中含Zn2+
D.锌作阴极,铁制品作阳极,溶液中含Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有4molHNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示.下列有关判断不正确的是( ) 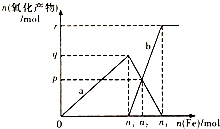
A.a是Fe(NO3)3
B.n1=1
C.p=1.2
D.n3=1.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于酸碱盐的说法正确的是( )
A. 化合物电离时,生成的阳离子有氢离子的是酸
B. 化合物电离时,生成的阴离子有氢氧根的是碱
C. 化合物电离时,只有生成金属阳离子与酸根离子的才是盐
D. 盐酸、稀硫酸、浓硝酸都能导电,但它们既不是电解质也不是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 用苯萃取溴水中的溴时,将溴的苯溶液从下口放出
B. NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体时即可停止加热
C. 蒸馏操作时,应该将温度计的水银球插入液面以下
D. 氧化钙中混有少量碳酸钙,可用盐酸除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X,Y,Z,W的原子序数依次增大,四种元素同周期,X的金属性再同周期元素中最强,Y原子的电子层数与最外层电子数相等;Z元素在地壳中的含量居于第二位,W的最高价氧化物的水化物的化学式为HnWO2n+2 , 下列说法正确的是( )
A.简单离子半径:X<Y<W
B.Y,Z两种元素的氧化物均具有两性
C.X,W分别形成的氢化物中所含化学键种类相同
D.Z,W形成化合物的电子式为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列五个反应
A.5Cl2+I2+6H2O=10HCl+2HIO3
B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
C.2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O
D.2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
E.MnO2+4HCl![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
上述反应中氯元素只被氧化的是_____________,(填字母,下同)只被还原的是_____________,部分被氧化的是_____________,C中被氧化与被还原的物质的量之比为_____________。
(2)在反应4(NH4)2SO4![]() N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为___________,生成56gN2转移的电子___________mol。
N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为___________,生成56gN2转移的电子___________mol。
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。上述反应中,若产生2mol N2,转移电子数为_________(用NA表示阿伏加德罗常数);用“双线桥”表示反应中电子转移,化合价的变化,反应类型:______________。
(4)将等质量的两份镁、铝合金分别投入足量的NaOH和HCl中,在相同的情况下测得生成气体的体积之比为1:2,求合金中镁、铝的物质的量之比为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com