
【题目】(1)下列五个反应
A.5Cl2+I2+6H2O=10HCl+2HIO3
B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
C.2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O
D.2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
E.MnO2+4HCl![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
上述反应中氯元素只被氧化的是_____________,(填字母,下同)只被还原的是_____________,部分被氧化的是_____________,C中被氧化与被还原的物质的量之比为_____________。
(2)在反应4(NH4)2SO4![]() N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为___________,生成56gN2转移的电子___________mol。
N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为___________,生成56gN2转移的电子___________mol。
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。上述反应中,若产生2mol N2,转移电子数为_________(用NA表示阿伏加德罗常数);用“双线桥”表示反应中电子转移,化合价的变化,反应类型:______________。
(4)将等质量的两份镁、铝合金分别投入足量的NaOH和HCl中,在相同的情况下测得生成气体的体积之比为1:2,求合金中镁、铝的物质的量之比为___________。
【答案】 D A B、C、E 5:1 1:3 12 20NA 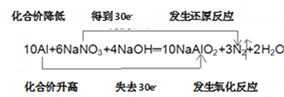 3:2
3:2
【解析】(1)反应A中氯元素化合价降低,被还原;反应B中氯气既是氧化剂,也是还原剂;反应C中氯元素化合价部分升高,被氧化;反应D中氯元素化合价升高,被氧化;反应E中氯元素化合价升高,被氧化;则上述反应中氯元素只被氧化的是D,只被还原的是A,部分被氧化的是B、C、E;根据方程式可知C中被氧化与被还原的物质的量之比为10:2=5:1;(2)在反应4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中氮元素化合价从-3价升高到0价,失去3个电子,氮气是氧化产物,硫元素化合价从+6价降低到+4价,得到2个电子,二氧化硫是还原产物,氧化产物与还原产物的物质的量之比为1:3,56gN2的物质的量是2mol,因此转移的电子的物质的量是2mol×6=12mol。(3)反应中氮元素化合价从+5价降低到0价,得到5个电子,因此若产生2mol N2,转移电子的物质的量是2mol×5×2=20mol,电子数为20NA;铝元素化合价从0价升高到+3价,失去3个电子,根据电子得失守恒可知电子转移的方向和数目可表示为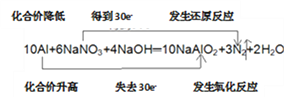 。(4)设镁的物质的量是xmol,铝的物质的量是ymol。镁只能与盐酸反应产生氢气,则生成的氢气是xmol。铝与盐酸或氢氧化钠反应生成的氢气均是1.5ymol,则
。(4)设镁的物质的量是xmol,铝的物质的量是ymol。镁只能与盐酸反应产生氢气,则生成的氢气是xmol。铝与盐酸或氢氧化钠反应生成的氢气均是1.5ymol,则![]() ,解得x:y=3:2。
,解得x:y=3:2。


科目:高中化学 来源: 题型:
【题目】下列各物质的分类、名称(或俗名)、化学式都正确的是 ( )
A. 氧化物 氧化铁 FeOB. 盐 胆矾 CuSO45H2O
C. 酸 硫酸 H2SD. 碱 纯碱 Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.10mol/L的硫酸950mL,某同学欲用密度为![]() 、溶质的质量分数为98%的浓硫酸进行配制。试回答:
、溶质的质量分数为98%的浓硫酸进行配制。试回答:
(1)需选用________容量瓶(填序号)。
A. 50 mL B. 100 mL C. 250 mL D. 1000 mL
(2)需量取98%浓硫酸的体积为_______mL。
(3)若提供如下仪器:
A. 量筒 B. 托盘天平 C. 玻璃棒 D. 容量瓶 E. 胶头滴管 F. 烧杯
完成该实验需选用哪些仪器?请按使用的先后顺序将仪器标号填在横线上:__________________。
(4)下列操作会使所配制的溶液物质的量浓度一定偏低的是_________。
A. 容量瓶洗净后未经干燥处理
B. 向容量瓶转移溶液时,有少量液体溅出
C. 量取浓硫酸时,仰视刻度线
D. 未洗涤烧杯玻璃棒
(5)下列关于容量瓶的使用方法中,正确的是_________(填序号)。
A. 使用前要检验是否漏水 B. 在容量瓶中直接溶解固体或稀释液体
C. 溶液未经冷却即注入容量瓶中 D. 向容量瓶中转移溶液要用玻璃棒引流
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,下列说法不正确的是
A. 蛋白质、淀粉和油脂都是天然高分子化合物
B. 烹鱼时加适量醋和酒可以增加香味
C. 工业上用电解熔融Al2O3的方法生产金属铝
D. 乙烯可作为水果的催熟剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,利用培养皿探究SO2的性质,实验时向Na2SO3固体上滴几滴浓硫酸,立即用另一表面扣在上面。表中对实验现象的描述或解释不正确的是
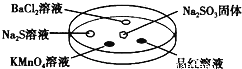
选项 | 实验现象 | 解释 |
A | BaCl2溶液变浑浊 | SO2与BaCl2溶液反应产生了BaSO3沉淀 |
B | Na2S溶液变浑浊 | SO2与Na2S溶液反应产生了S单质 |
C | 酸性KMnO4溶液褪色 | SO2具有还原性 |
D | 品红溶液褪色 | SO2具有漂白性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CuC12和FeC12的混合溶液中,加入一定量的锌粉,充分反应后过滤,向滤渣中加稀盐酸,有气体生成,则滤渣中一定含有
A. Cu、Fe和ZnB. Cu和FeC. Zn和CuD. Fe和Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件下,两瓶气体所含原子数一定相等的是( )
A. 同压强、同体积的N2O和CO2 B. 同温度、同体积的H2和N2
C. 同体积、同密度的CH4和C3H6 D. 同质量、不同密度的N2和CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量CO2通入KOH和Ca(OH)2的混合稀溶液100mL中,生成沉淀的质量(m)与通入(STP)状况下CO2的体积(V)之间关系如图所示:
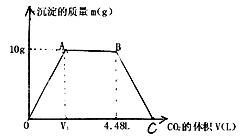
(1)写同下列各段发生的离子方程式
①OA_____________________ ;
②AB_____________________;
③BC_____________________;
(2)C点对应溶液中溶质离子有:_____________________;
(3)V1=_________________L;
(4)KOH物质的量浓度c=____________________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com