
【题目】对于密闭容器中进行的反应:P(g)+ Q(g)![]() R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
A. P、Q、R、S的浓度相等
B. P、Q、R、S在密闭容器中共存
C. P、Q、R、S的浓度不再变化
D. 用P的浓度表示的化学反应速率与用Q的浓度表示的化学反应速率相等。
科目:高中化学 来源: 题型:
【题目】国产航母001A等舰艇的船底都涂有含Cu2O的防污涂料,制备Cu2O的一种方法为:Zn+2CuSO4+2NaOH===Cu2O+ZnSO4+Na2SO4+H2O。该反应的下列说法正确的是( )

A. Zn得到电子
B. CuSO4被氧化
C. NaOH是还原剂
D. CuSO4是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目要求填空:
(1)硫、氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨.用化学方程式表示NO2形成酸雨的原因: , 该反应中氧化剂和还原剂的物质的量之比为 .
(2)实验室常用的几种气体发生装置如图1A、B、C所示: 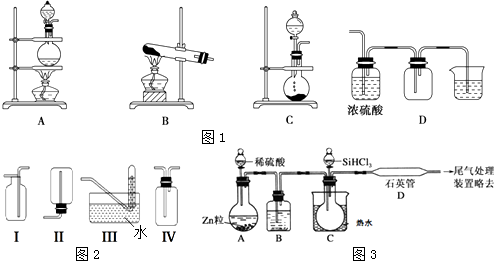
实验室可以用B或C装置制取氨气,如果用B装置,反应的化学方程式是;如果用C装置,通常使用的药品是(写名称);图2是某学生设计收集氨气的几种装置,其中可行的是 . 若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的
A.CO2 B.NO C.Cl2 D.H2
写出A装置中反应的离子方程式 .
(3)氢化钠(NaH)是一种还原性极强的物质,广泛应用于工业生产.
氢化钠(NaH)中Na元素的化合价为+1,在高温下氢化钠(NaH)可将四氯化钛(TiCl4)还原成金属钛,该反应的化学方程式为 .
NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,NaH与液氨(NH3)也有类似反应,该反应的化学方程式为 . 如果有12g NaH参加此反应,则转移电子的物质的量为mol
(4)用SiHCl3与过量H2反应制备纯硅的装置如图3所示(热源及夹持装置均已略去):
SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式:;H2还原SiHCl3过程中若混入O2 , 可能引起的后果是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时将浓度均为0.1mol·L-1、体积分别为Va和Vb的HA 溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示,下列说法正确的是
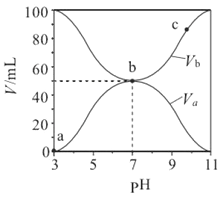
A. a→c 过程中水的电离程度始终增大
B. b点时,c(B+)=c(A-)=c(H+)=c(OH-)
C. c点时, 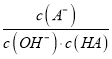 随温度升高而减小
随温度升高而减小
D. 相同温度下,Ka(HA)>Kb(BOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质与条件已略去)。A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物;I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中。

请回答下列问题:
(1) H的化学式为________________。
(2) D的电子式为________________。
(3) 写出反应①的化学方程式:________________。
(4) 写出G的水溶液与C的硝酸盐溶液反应的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键与晶体结构说法正确的是
A.两种元素组成的分子中一定只有极性键
B.离子化合物的熔点一定比共价化合物的高
C.非金属元素组成的化合物一定是共价化合物
D.含有阴离子的化合物一定含有阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 95 ℃纯水的pH<7,说明加热可导致水呈酸性
B. pH=3的盐酸溶液,加水稀释至溶液体积为原来体积10倍后pH=4
C. pH=1的盐酸与等体积pH=3的盐酸混合后pH=2
D. pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com