
| A����������ά�Ҵ����������Ʒ�ͣ������ڻ������������ij�Ʒ������ |
| B����һ��Ŀ����ʹ�ո������õ���ѧ���ã�������Ϊ���ҽ�Լ������ʳ |
| C���Ҵ��ܲ����������������ȼ������Ϊ�Ҵ����������Ԫ����ͬ����ѧ�ɷ����� |
| D������10%ȼ���Ҵ����Ҵ����Ϳ���ʹ����β����һ����̼�ŷ����½� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| �ζ����� | ������Һ�����mL�� | ������� | |
| �ζ�ǰ�Ŀ̶ȣ�mL�� | �ζ���Ŀ̶ȣ�mL�� | ||
| ��һ�� | 10.00 | ��.���� | ����.���� |
| �ڶ��� | 10.00 | ��.���� | ����.���� |
| ������ | 10.00 | ��.���� | ����.���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Һ��pH���� | B��CH3COOH����̶ȱ�� |
| C����Һ�ĵ����������� | D����Һ��c(OH��)��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ͬ�¶��£�1 mol��L-1������Һ��0.5 mol��L-1������Һ�У�c��H+��֮����2��1 |
| B�����������Һ�м����������ᣬʹ���Һ��pH=7����ʱ���Һ��c��Na+��=c��CH3COO-�� |
| C��pH=3������ʹ����ˮʹ��Һ����ֱ�����100����pH����ͬ |
| D��0.1 mol��L-1NH4Cl��Һ��c(NH4+)+c��H+��=c��Cl-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
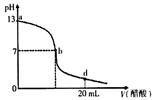
| A��������������Һ�����ʵ���Ũ��Ϊ0.1 mol/L �� |
| B����b�㣬c (Na+��=c(CH3COO-�� |
| C����d�㣬��Һ����������Ũ���ɴ�С��˳��Ϊ c (CH3COO-��>c (Na+)>c (H+��>c (OH-�� |
| D������������Һ�������Һǡ����ȫ��Ӧ�ĵ�λ������b��d���ij�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������ƾ���Ƴ�ȼ�ϵ�أ�����Ϊȼ�ϵ�ؾ��нϸߵ����������ʣ�ͬʱ�������ƾ���ȼ�Ͽ����� |
| B�����������ḻ��ú̿��Դ������ú�����������������ú���ۺ������ʣ��ɼ��ٶ�ʯ�͵����� |
| C������������̫���ܡ��������ܡ����ܵȣ������ҹ��������غ������˽�̫���ܡ���������վ�� |
| D�������������ú���ȼ�������ڻ��⻯ʯ��Դ��ȱ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 �ľ���ֵ����ȷ��
�ľ���ֵ����ȷ��| A��C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g)����H=" ��1367.0" kJ/mol��ȼ���ȣ� |
| B��NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l)����H=" +" 57.3kJ/mol���к��ȣ� |
| C��P(s)+ 3/2 Cl2(g)="==" PCl3(g)����H=" ��306" kJ/mol����Ӧ�ȣ� |
| D��2NO2==O2+2NO����H=" +" 116.2kJ/mol����Ӧ�ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��40 mL | B��72 mL | C��80 mL | D��128 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��4��5 | B��1��10 | C��10��1 | D��1��2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com