
����Ŀ��Ϊ��Ч�������������ػ�����ȡ��ʩ���ƴ����������о�����Ч���ƿ����еĵ������̼������ĺ����Ե���Ϊ��Ҫ��
I.���������о�
��1��һ�������£���2molNO��2molO2���ں����ܱ������з�����Ӧ2NO(g)+O2(g)![]() 2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬���� ________________������ĸ���ţ� ��
2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬���� ________________������ĸ���ţ� ��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��NO��O2�����ʵ���֮�ȱ��ֲ��� d��ÿ����1 molO2ͬʱ����2 molNO2
��2��������ȼ������ʱ������N2��O2�ķ�Ӧ��N2 +O2![]() 2NO���ǵ�������β���к���NO��ԭ��֮һ����T1��T2�¶��£�һ������NO�����ֽⷴӦʱN2�����������ʱ��仯����ͼ��ʾ������ͼ���жϷ�ӦN2(g)+O2(g)
2NO���ǵ�������β���к���NO��ԭ��֮һ����T1��T2�¶��£�һ������NO�����ֽⷴӦʱN2�����������ʱ��仯����ͼ��ʾ������ͼ���жϷ�ӦN2(g)+O2(g)![]() 2NO(g)����H__________0(����������������)��
2NO(g)����H__________0(����������������)��

����̼�������о�
��1������ɱ䣨����������֮���Ħ�������Բ��ƣ����ܱ���������ͼ��ʾ���ֽ�3molH2��2molCO���������У��ƶ����������VΪ2L����í���̶���A��B�㣬�����ϳɼ״��ķ�Ӧ���£�CO(g)+2H2(g)![]() CH3OH(g)��
CH3OH(g)��
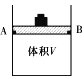
�ⶨ��ͬ��������ͬʱ����ڵ�CO��ת���ʣ��õ��������ݣ�
T������ | 10min | 20min | 30min | 40min |
T1 | 20% | 55% | 65% | 65% |
T2 | 35% | 50% | a1 | a2 |
�������ϱ����ݣ���Ƚ�T1_________T2(ѡ����>������<������=��)��T2���£���30min ʱ��a1=________�����¶��µĻ�ѧƽ�ⳣ��Ϊ__________________��
��T2���£���40minʱ����ȥí���������ܷ������ã�����û�з����ƶ�������������ͨ��6molCO����ʱv(����________v(�棩(ѡ����>������<����
��2��һ�������¿��ü״���CO��Ӧ���ɴ�������CO��Ⱦ�������£���a mol/L�Ĵ�����b mol/L Ba(OH)2��Һ��������(��Ϻ���Һ����仯���Բ��ƣ�����ַ�Ӧ����Һ�д���2c(Ba2+)��c(CH3COO-)���������Һ�еĵ��ƽ���֪����Һ��pH=___________��������������ĵ��볣��Ka =____________ (�ú�a��b�Ĵ���ʽ��ʾ����
���𰸡� abc > < 50% 4��4(mol/L)-2 ��4(L/mol)2 < 7 2��10-7b/(a-2b) mol/L
����������(1)�����ܱ������з�����Ӧ��2NO(g)+O2(g)2NO2(g)��a����Ӧ�Ǹ���������ı�ķ�Ӧ������������ѹǿ�ı䣬ƽ��ʱ����ϵѹǿ���ֲ��䣬����ȷ��b�����������ɫ���ֲ��䣬˵������������Ũ�ȱ��ֲ��䣬�ﵽƽ�⣬����ȷ��c��NO��O2����ʼ���ʵ�����ȣ�����ѧ��������ͬ���仯���Ͳ���ͬ�����û�дﵽƽ�⣬NO��O2 �����ʵ���֮�Ȼᷢ���ı䣬�������ı�˵��������ƽ�⣬����ȷ��d��O2 �Ƿ�Ӧ�NO2��������������κ�ʱ����ÿ����1 molO2ͬʱ����2 molNO2���ʴ���ѡ��abc��
(2)��ͼ��֪�ȴﵽƽ������ʱ��϶̵��¶Ƚϸߣ��Ҵ��¶��µ��������������С��˵���¶����ߺ�Ӧ�����ƶ����ʷ�ӦΪ���ȷ�Ӧ���ʴ�Ϊ������
����(1)�������¶ȣ���ѧ��Ӧ���ʼӿ죬10min�ڣ�T2ʱCOת���ʴ���T1ʱ����T1��T2��
T2���£�10minʱCO2ת����Ϊ35%��20minʱCO2ת����Ϊ50%��10-20minֻת��15%��˵��20minʱ�Ѵ�ƽ��״̬���ʵ�30minʱ��CO2ת����Ϊ50%��
T2���£�CO(g)+2H2(g) ![]() CH3OH(g)��
CH3OH(g)��
��ʼ(mol) 2 3 0
ת��(mol) 1 2 1
\ƽ��(mol) 11 1
��ѧƽ�ⳣ��K=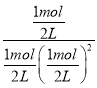 =4���ʴ�Ϊ������50%��4��
=4���ʴ�Ϊ������50%��4��
�ڰ�ȥí������������ͬ��ͬѹ�½��У����֮�ȵ������ʵ���֮�ȣ�������6molCO������ƽ�ⲻ�ƶ�����ʱ���������Ϊ6L��Qc=![]() =
=![]() ��K����ƽ�������ƶ���v(��)��v(��)���ʴ�Ϊ������
��K����ƽ�������ƶ���v(��)��v(��)���ʴ�Ϊ������
(2)��Ӧƽ��ʱ��2c(Ba2+)=c(CH3COO-)=bmol/L���ݵ���غ㣬��Һ��c(H+)=c(OH-)=10-7mol/L����Һ�����ԣ��������ƽ�ⳣ�����ݵ��뷽��ʽд��K=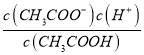 =
=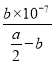 =
=![]() ��107mol/L���ʴ�Ϊ��7��
��107mol/L���ʴ�Ϊ��7�� ![]() ��107mol/L��
��107mol/L��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¸��������£����е��뷽��ʽ����д��ȷ����
A������״̬�µ�NaHSO4���룺NaHSO4=Na����H����SO42��
B��H2CO3�ĵ��룺H2CO3![]() 2H����CO32��
2H����CO32��
C��Fe(OH)3�ĵ��룺Fe(OH)3![]() Fe3����3OH��
Fe3����3OH��
D��ˮ��Һ�е�NaHSO4���룺NaHSO4=Na����HSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��![]() ��
��![]() N��
N��![]() O��
O��![]() Cl��
Cl��![]() U��
U��![]() U��
U�У�
��1��___��_____����������ȣ������ܻ���Ϊͬλ�ء�
��2��___��____����������ȣ�������������ȣ����Բ���ͬһ��Ԫ�ء��������й���______��Ԫ�ء�
��.���ʵ����ͺ���Ԫ�صĻ��ϼ����о��������ʵ����������ӽǡ�

��3��Y�ķ���ʽΪ________��
��4��ͼ��X�ĵ���ʽΪ![]() ����ˮ��Һ�����ڿ����з������ױ���ǣ�ԭ����________(�û�ѧ����ʽ��ʾ)���ñ仯���ֳ���S�ǽ����Ա�O____(����ǿ����������)����ԭ�ӽṹ����ԭ��ͬ����Ԫ�ش��ϵ��£�__________���õ�������������
����ˮ��Һ�����ڿ����з������ױ���ǣ�ԭ����________(�û�ѧ����ʽ��ʾ)���ñ仯���ֳ���S�ǽ����Ա�O____(����ǿ����������)����ԭ�ӽṹ����ԭ��ͬ����Ԫ�ش��ϵ��£�__________���õ�������������
��5��Z��ͼ����ij���ʷ�Ӧ����SO2�Ļ�ѧ����ʽ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������(Na2S2O4)�׳Ʊ��շۣ���һ��Ư�����������ͷ�������ij�о�С���Na2S2O4���������Ʊ�����������̽����
��1���ⶨ0.05mol��L��1 Na2S2O4��Һ�ڿ�����pH�ı仯��ͼ��ʾ��
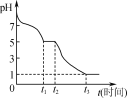
��д��0��t1�η�����Ӧ�Ļ�ѧ����ʽ��_____��
��t2��t3����Һ��pH��С��ԭ����______��
��2����֪��S2O32-��2H��===SO2����S����H2O��Na2S2O4�����ڸ��������������¼�����75��������ȫ�ֽ�õ�Na2SO3��Na2S2O3��SO2������������Ƿ���Na2SO4��ʵ�鷽����__________��
��3���ɹ�ҵ�����Ʊ�Na2S2O4��ʵ��ԭ�����£�
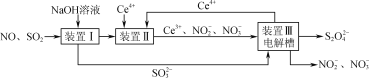
����װ�â��м���Ce4����Ŀ����________��
��д��װ�â��з�����Ӧ�����ӷ���ʽ��________��
��4����п�۷��Ʊ�Na2S2O4��ʵ��װ����ͼ��ʾ����Ҫ�������£�

����1����SO2ͨ��п�۵�ˮ����Һ�У���35��45���·�Ӧ��������������п��
����2����������ռ���Һ����28��35 ���·�Ӧ����Na2S2O4��������п������Һ��
������ʵ���һ���ᴿ�õ�Na2S2O4(s)��ʵ�鷽����ȡһ������Na2S2O4��������п������Һ��______(ʵ������ʹ�õ��Լ��У��Ȼ��ơ��Ҵ�����������������ʹ�õ������У���ո�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2���黯��һ��ʵ��CO2��Դ�����õ���Ч;����
���Ȼ�ѧת��
CO2���黯���̷�����Ӧ��CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)��H
CH4(g)+2H2O(g)��H
(1)ÿ����1mol CH4(g)������165 kJ������H��______��
(2)��Ӧ��ƽ�ⳣ���ı���ʽ��K��______���¶����ߣ�K______(����������������С��)��
(3)������������ʱ��һ��ʱ���ڣ�ѹǿ��CO2��ת���ʼ�CH4��ѡ���Ե�Ӱ������ͼ��

ע��ѡ���ԣ�ת��ΪĿ������ԭ������ԭ���ܵ�ת����
CO2���黯��Ӧѡ��0.1MPa����ѡ�����ѹǿ��ԭ����______��
�绯ѧת��
�ྦྷCu�ɸ�Ч��CO2���黯�����CO2�Ʊ�CH4��ԭ��ʾ��ͼ���¡����������¶ȿ�����10�����ң�����ͨ��CO2�����������ҵ�KHCO3��Һ��Ũ�Ȼ������ֲ��䡣

(4)�ྦྷCu��______(����������������)����
(5)��ϵ缫��Ӧʽ��˵��������KHCO3��ҺŨ�Ȼ��������ԭ��______��
(6)�����������в�ȡ��______��ʩ(д2������)ʹCO2������H+�ŵ硣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��ȷ����
A. Fe(OH)3��HI�ķ�Ӧ��Fe(OH)3��3H��==Fe3����3H2O
B. 1.5 mol/L 100 ml��FeBr2��Һ��ͨ��3.36L����״����Cl2��2Fe2++2Br��+2Cl2==2Fe3++4Cl��+Br2
C. ����������ϡ������Һ��Ӧ�ų�NO���壺3Fe��8H����2NO3-==3Fe2����4H2O��2NO��
D. ������[KAl(SO4)2]��Һ����μ���Ba(OH)2��Һ��SO42��ǡ�ó�����ȫ��2Al3����3SO42����3Ba2����6OH��==2Al(OH)3����3BaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȼ�յķ�ӦΪ��P4 + 5O2 = P4O10����֪���л�ѧ���ļ��ֱܷ�Ϊ��P��P a kJ��mol-1��P��O b kJ��mol-1��P=O c kJ��mol-1��O=O d kJ��mol-1������ͼʾ�ķ��ӽṹ���й����ݣ������ƶ���ȷ����

A��6a+5d < 4c + 10b
B����H = (4c+12b��6a��5d) kJ��mol-1
C��6a+5d > 4c + 12b
D����H = (6a+5d��4c��12b) kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1molN2�����3molH2������2L�ĺ��������У�����һ�������·������·�Ӧ��N2(g)+3H2(g) ![]() 2NH3(g)������2s����NH3��Ũ��Ϊ0.6mol��L-1���������м���˵�������в���ȷ����
2NH3(g)������2s����NH3��Ũ��Ϊ0.6mol��L-1���������м���˵�������в���ȷ����
A. ��N2��ʾ�ķ�Ӧ����Ϊ0.15mol��L-1��s-1 B. 2sʱH2��ת����Ϊ40��
C. 2sʱN2��H2��ת������� D. 2sʱH2��Ũ��Ϊ0.6mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���F��һ�ֹؽ���ֹʹҩ���ϳ�F��һ�ִ�ͳ����·�����£�
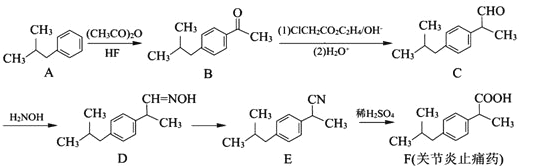
��1��B�к��������ŵ�����Ϊ_________��
��2��C��D�ķ�Ӧ�ɷ�Ϊ�������䷴Ӧ����Ϊ_________��_________��
��3��д����F��5��̼ԭ�ӵ�ͬϵ��X�Ľṹ��ʽ��_______________��дһ�֣���X�ж���ͬ���칹�壬��������������X��ͬ���칹�干��_______________�֡�
�����ڷ����廯����ڱ�����ֻ��1��ȡ�������������������ʣ�
��4��д��Eת��ΪF�����εĻ�ѧ����ʽ��______________________��
��5����֪����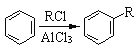
�� 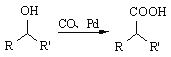 ��R1��R2��ʾ������
��R1��R2��ʾ������
�ϳ�F��һ�ָ���������2������1������[(CH3)2CHCH2OH)]������������[(CH3CO)2O]Ϊԭ�����ϳɣ�д���йصĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�H2C��CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH__________________
CH3CH2OH__________________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com