
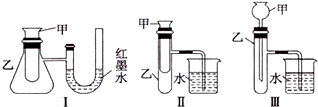
分析 (1)装置Ⅰ和Ⅱ都可以分别通过右边装置中液面变化、是否有气泡判断反应是吸热还是放热,而装置Ⅲ是将生成的气体直接通入水中,无法判断该反应是吸热还是放热反应;
(2)酸碱中和反应为放热反应,反应放出的热使锥形瓶中温度升高,气体体积增大,据此判断U型管中液面的变化;
(3)①钠与水的反应为放热反应,温度升高导致大试管中气体受热压强增大,烧杯中有气泡产生,冷却后体积减小,压强减小,导管中会形成水柱;
②若只观察到烧杯里的玻璃管内形成一段水柱,说明M溶于水后导致大试管中温度降低,压强减小;
解答 解:(1)装置Ⅰ可通过U形管中红墨水液面的变化判断铜与浓硝酸的反应是放热还是吸热;装置Ⅱ可通过烧杯中是否产生气泡判断铜与浓硝酸的反应放热还是吸热;装置Ⅲ只是一个铜与浓硝酸反应并将生成的气体用水吸收的装置,不能证明该反应是放热反应还是吸热反应,
故答案为:Ⅲ;
(2)氢氧化钡与硫酸反应属于中和反应,中和反应都是放热反应,所以锥形瓶中气体受热膨胀,导致U型管左端液柱降低,右端液柱升高,
故答案为:左端液柱降低,右端液柱升高;放热;
(3))①若M为钠,钠与水反应生成氢氧化钠和氢气,该反应为放热反应,放热的热量使大试管中温度升高,气体压强增大,所以右边烧杯中有气泡产生,反应完毕后,冷却至室温,烧杯里的导管内形成一段水柱,
故答案为:产生气泡,反应完毕后,冷却至室温,烧杯里的导管内形成一段水柱;
②若观察到烧杯里的玻璃管内形成一段水柱,说明M溶于水后导致大试管中温度降低,压强减小,证明M溶于水为吸热过程,溶于水能够吸收热量的物质有:硝酸铵、氯化铵等,
故答案为:硝酸铵;
点评 本题考查化学反应中的热效应,题目难度中等,注意掌握探究反应热效应的常用方法,试题有利于培养学生实验综合分析能力,特别是实验的评价和根据实验现象推理的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯化氢气体溶于水 | B. | 白磷在一定条件下转化为红磷 | ||
| C. | 碘在加热条件下升华 | D. | 氯化钠晶体加热熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有化合价变化的化学反应一定是氧化还原反应 | |
| B. | 离子反应方程式比化学方程式更能描述化学反应的本质 | |
| C. | 钠能和水反应置换出氢气,也能和硫酸铜溶液反应置换出铜 | |
| D. | 有单质参加的化合反应和有单质生成的分解反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某地燃烧化石燃料排放的废气中含CO2、SO2,使雨水pH=6形成酸雨 | |
| B. | 氟利昂和NOX都能破坏臭氧层,从而导致“温室效应” | |
| C. | 中国是目前全球最大的稀土生产国和出口国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径 | |
| D. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解气和水煤气的主要成分都是甲烷 | |
| B. | 石油分馏是化学变化,可得到汽油、煤油 | |
| C. | 化石燃料所存贮的大量能量,实质是来源于太阳能 | |
| D. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
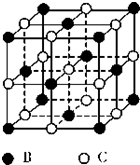 有A、B、C、D、E五种原子序数依次增大的元素(原子序数均不大于30).A的基态原子2p能级有3个单电子;C的核外没有成单电子,B、C两元素形成的化合物晶胞结构如图所示;D的3p能级有1个单电子,且与B所在主族相邻;E元 素在地壳中含量居第四位;则:
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均不大于30).A的基态原子2p能级有3个单电子;C的核外没有成单电子,B、C两元素形成的化合物晶胞结构如图所示;D的3p能级有1个单电子,且与B所在主族相邻;E元 素在地壳中含量居第四位;则:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
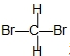 和
和 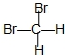
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com