
����Ŀ����T �������£���1 L�̶�������ܱ�����M�м���2 mol X��1 mol Y���������·�Ӧ��2X(g)��Y(g)![]() a Z(g)��W(g)����H����Q kJ��mol��1(Q��0��aΪ������)������Ӧ�ﵽƽ���Ӧ�ų�������ΪQ1 kJ������X��ת����Ϊ������ƽ����������¶ȣ���������ƽ����Է���������С����
a Z(g)��W(g)����H����Q kJ��mol��1(Q��0��aΪ������)������Ӧ�ﵽƽ���Ӧ�ų�������ΪQ1 kJ������X��ת����Ϊ������ƽ����������¶ȣ���������ƽ����Է���������С����
(1)��ѧ������a��ֵΪ________��
(2)����˵������˵���÷�Ӧ�ﵽ�˻�ѧƽ��״̬����________��
A��������ѹǿһ���������� B��������������ܶ�һ��
C��������Z������һ�� D�����������������һ��
(3)�¶�ά��T �治�䣬����ʼʱ������M�м�������ʵ��������и����Ӧ�ﵽƽ���ų���������ΪQ1 kJ����________(ϡ�����岻���뷴Ӧ)��
A��2 mol X��1 mol Y��1 mol Ar
B��a mol Z��1 mol W
C��1 mol X��0.5 mol Y��0.5a mol Z��0.5 mol W
D��2 mol X��1 mol Y��1 mol Z
(4)�¶�ά��T �治�䣬����ʼʱ������M�м���4 mol X��6 mol Y�����ﵽƽ��ʱ�����ڵ�ѹǿ��С��10%����Ӧ�зų�������Ϊ________kJ��
(5)�¶�ά��T �治�䣬����һ����ԭ���������ȵĺ�ѹ����N �У�����2 mol X��1 mol Y�������Ϸ�Ӧ����ƽ�⣬��________(ѡ��M��N)�����еķ�Ӧ�ȴﵽƽ��״̬��������X����������M________N(ѡ�������������)��
(6)��֪���÷�Ӧ��ƽ�ⳣ�����¶ȵı仯���±���
�¶�/�� | 200 | 250 | 300 | 350 |
ƽ�ⳣ��K | 9.94 | 5.2 | 1 | 0.5 |
����ij�¶��£�2 mol X��1 mol Y������M�з�Ӧ��ƽ�⣬ X��ƽ��ת����Ϊ50%������¶�Ϊ________�档
���𰸡�1ACAQN��350
��������
��1����Ӧ���ȣ���ƽ����������¶ȣ���ƽ�������ƶ�����������ƽ����Է���������С��˵����Ӧ������Ļ�ѧ������֮�ʹ�������������Ļ�ѧ������֮�ͣ���2+1��a+1����a=1���ʴ�Ϊ��1��
��2��A.���ڷ�Ӧǰ������Ļ�ѧ������֮�Ͳ���ȣ���ƽ��ʱѹǿ���ٷ����仯����A��ȷ��B.�������ڹ̶�����������з�Ӧ���������Ƿ�ﵽƽ��״̬���ܶȶ����䣬��B����C.��Ӧ�ﵽƽ��״̬ʱ�����ʵ�Ũ�ȡ������������Ȳ��ٷ����仯����ƽ��ʱ������Z������һ������C��ȷ��D.��Ӧ��������ﶼ�����壬�����Ƿ�ﵽƽ��״̬�������������������һ������D���ʴ�Ϊ��AC��
��3��������������䣬����ϡ�������ƽ����Ӱ�죬�ų����������䣬��A��ȷ����Ӧ���淴Ӧ��ʼ����Ӧ������������B����C����ʼ����������ɵ�Ч���������������ƽ��ʱ�ų���������С��Q1kJ����C����D���൱��ԭƽ��ʱ������Z��ƽ�������ƶ�����ƽ��ʱ�ų���������С��Q1kJ����D���ʴ�Ϊ��A��
��4����ת����X�����ʵ���Ϊ2amol�����У�
2X(g)+Y(g)![]() Z(g)+W(g) ��H=-QkJmol-1(Q��0)
Z(g)+W(g) ��H=-QkJmol-1(Q��0)
��ʼ(mol) 4 6 0 0
ת��(mol) 2a a a a
ƽ��(mol) 4-2a 6-a a a
��ǰ���ѹǿ֮�ȵ������ʵ���֮�ȿɵã�![]() =90%����a=1����ת����XΪ2mol�����Ȼ�ѧ����ʽ�ɵô�ʱ�ų�������ΪQkJ���ʴ�Ϊ��Q��
=90%����a=1����ת����XΪ2mol�����Ȼ�ѧ����ʽ�ɵô�ʱ�ų�������ΪQkJ���ʴ�Ϊ��Q��
��5���������£���ѹ�������ȣ��൱������ѹǿ��ѹǿԽ��Ӧ����Խ��Ӧ����ƽ���ʱ��Խ�̣�����ѹǿƽ��������Ӧ�����ƶ�����X������������С���ʴ�Ϊ��N������
��6��2molX��1molY������M�з�Ӧ���ﵽƽ�⣬x��ƽ��ת����Ϊ50%��
2X��g��+Y��g��![]() Z��g��+W��g��
Z��g��+W��g��
��ʼ��mol����2 1 0 0
ת����mol����1 0.5 0.5 0.5
ƽ�⣨mol����1 0.5 0.5 0.5
ƽ�ⳣ��k=![]() =
=![]() =0.5�� �������¶���350�棬�ʴ�Ϊ��350����
=0.5�� �������¶���350�棬�ʴ�Ϊ��350����


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʳ�ַ�Ӧ����ˣ�����Һ���ȡ��������������䣬���ղ��ܵõ����������( )
A. ��1 mol Ca(HCO3)2����Һ�м���1 mol Na2O2
B. ���������Ĥ����Ƭ�м�������
C. ��Ư����Һ��ͨ�����CO2
D. ��1 mol KAl(SO4)2����Һ�м���2 mol Ba(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ����dz�����ˮ����������ҵ���Ʊ���ˮFeCl3��һ�ֹ������£�
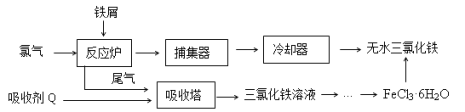
��1����FeCl3�� 6H2O�����Ʊ���ˮFeCl3Ӧ��ȡ�Ĵ�ʩ�ǣ� ��
��2����ˮ���Ȼ�����ˮ�е��ܽ�����£�
�¶�/�� | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
�ܽ����g/100gH2O�� | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
��FeCl3��Һ�Ƶ�FeCl3��6H2O����IJ��������ǣ������������ᡢ �� �����ˡ�ϴ�ӡ����
��3�������£�����Һ��pH���Ʋ�����ʹFe3+������pH��4ʱ����Һ��c��Fe3+���� mol��L-1����������Ksp[Fe��OH��3]��2.6��10-39����
��4��FeCl3����������ͨ�����õ������ⶨ����ȡ2.300g��ˮ�Ȼ�����Ʒ������ϡ���ᣬ ��ת�Ƶ�100mL����ƿ��������ˮ������ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ����ijһָʾ������0.1000mol��L-1Na2S2O3��Һ�ζ���ȥ12.50mL��
��֪��I2��2S2O32����2I����S4O62-
�� д�������Թ�����KI��Һ��Ӧ�����ӷ���ʽ�� ��
�� ����Ʒ���Ȼ���������������д�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��������ͼ��ʾװ�������Ũ�����SO2������ʵ��(�г�װ����ʡ��)����ش���������

(1)������״��ͭ˿����Ũ�����У�������Ӧ�Ļ�ѧ����ʽΪ____________��
(2)ʵ���У��Թܢ��е�Ʒ����Һ_____________(������)��
(3)����˵������ȷ����_______(����ĸ����)
A.��Ӧ���Թ�I�е�Һ����μ���ˮ�У���Һ����ɫ B.�Թܢ��г��ְ�ɫ����
C.�Թܢ��е�����KMnO4��Һ��ɫ D.�Թ�V�е�NaOH��Һ��������β��
(4)����Ӧ����0.02 mol H2SO4����ԭ����Ӧ�������������Ϊ______mL(��״����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. 24 g þ��27 g���У�������ͬ��������
B. ͬ�������������ͳ����У���������ͬ
C. 1 mol��ˮ��1 molˮ�У���������Ϊ2��1
D. 1 mol�����1 mol��ϩ�У���ѧ������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�ѧ��Ӧ�е������仯������˵���в���ȷ����( )
A. ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ
B. ���ڿ��淴Ӧ��aA(g)+bB(g)![]() bC(g)+dD(g)���������Ӧ���ȣ��淴Ӧһ������
bC(g)+dD(g)���������Ӧ���ȣ��淴Ӧһ������
C. ����ȼ������ˮ��һ�����ȵĻ�ѧ��Ӧ��˵��1 mol H2����������1 mol H2O������
D. ֻ�з��ȵ�������ԭ��Ӧ�ſ������Ϊԭ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ![]() ����H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��
����H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��

�ش����⣺
�ŷ�Ӧ�Ļ�ѧ����ʽ��a��b��cΪ��
�ƣ���ƽ����Ӧ����v����A����v����A����v����A���Ӵ�С���д���Ϊ��
�ǣµ�ƽ��ת���ʦ�����B����������B����������B������С���ǣ���ֵ�ǣ�
���ɵ�һ��ƽ��ڶ���ƽ�⣬ƽ���ƶ��ķ����ǣ���ȡ�Ĵ�ʩ�ǣ�
�ɱȽϵڢ�η�Ӧ�¶����������͵ڢ�η�Ӧ�¶����������ĸߵͣ�������������������������������жϵ������ǡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��100mL�ܶ�Ϊ1.84g/cm3����������Ϊ98%��Ũ�����У�c(H2SO4����( )
A. 18.4 B. 9.8mol��L��1 C. 1.84mol��L��1 D. 18.4mol��L��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com