
| A�� | �ݢڢۢ٢ޢܢ� | B�� | �ݢ٢ڢۢޢܢ� | C�� | �ݢڢ٢ۢܢޢ� | D�� | �ݢۢڢ٢ޢܢ� |
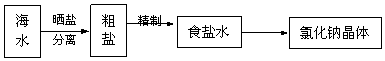
���� �����ܽ���Σ�Ȼ��ѡ��̼������Һ��ȥ�����ӡ���ȥþ���ӡ�������ѡ������������Һ����ȥ���������ѡ���Ȼ�����Һ��Ϊ�˱�֤�����ʳ����������Լ����������Ϊ�˲������µ����ʣ�Ӧ���ȼ����������ƣ�Ȼ������Ȼ������ټ���̼���ƣ���������������ÿ���Լ������������֤���������ʶ��ܳ�ȥ����Ӧ����ü��ȷ�������ȥʣ����Ȼ��⣬�Դ˽����⣮
��� �⣺�����ܽ⣬Ȼ���ȼ���������NaOH����ȥþ���ӡ������ӣ�Ȼ��������BaCl2����ȥSO42-��CO32-���ټ������Na2CO3 ��ȥCa2+������Ba2+�����˺���Һ�м�����������ᣬ��ȥ��Һ��ʣ���̼��������������е��������������ȳ�ȥʣ����Ȼ��⣬Ҳ���ȼ�BaCl2���ټ���NaOH����Ӧ��֤��������μ���Na2CO3��HCl���ʺ���˳���ǣ��ݢۢڢ٢ޢܢ��ߢݢڢۢ٢ޢܢߣ�
��ѡAD��
���� ���⿼���˴��ε��ᴿ��Ϊ��Ƶ���㣬������ѧ���ķ���������ʵ�������Ŀ��飬��һ�����ʵķ�����ᴿ�ķ����ͻ����������ۺ�Ӧ���⣬ע�����ʵ��Ŀ����Ժͺ����Ե����ۣ��Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ֤���ˣ������Ԫ�صĻ����һ������ǿ������ | |
| B�� | 1mol��ԭ����Ӧʱ��ת�Ƶĵ�����Ϊ2NA | |
| C�� | H2SO4�ڷ�Ӧ�б����������Ժ����� | |
| D�� | �������ø÷�Ӧԭ����������Ƴ�ԭ��أ�ͨ��������ǿ���ж�˾���Ƿ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶���ʹ��ѧ��Ӧ����������Ҫԭ���������˷�Ӧ������л���Ӱٷ��� | |
| B�� | ������μӵĻ�ѧ��Ӧ������ѹǿ������С��Ӧ������������������ӷ�Ӧ������л���ӵİٷ����Ӷ�ʹ��Ӧ�������� | |
| C�� | ����Ӧ��Ũ�ȿ�����λ����ڻ���ӵİٷ������Ӷ�ʹ��Ч��ײ�������� | |
| D�� | ������Ӱ�췴Ӧ�Ļ�ܣ���������λ����ڻ���Ӱٷ���������Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
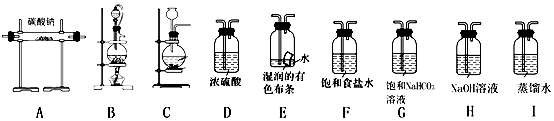
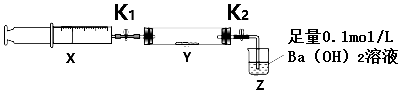
| �������� | ʵ������ | ����ԭ�� |
| ��K1���ƶ�ע����������ʹX�е����建��ͨ��Y���У������ַ�Ӧ�� | �ٵ���ɫ�����Ϊ��ɫ��ĩ | �ڷ�Ӧ�Ļ�ѧ����ʽ2Na2O2+2CO2=2Na2CO3+O2 |
| ��ע���������˻�ԭ�����̶�����װ�ûָ������£���K2 | ��Z��Һ����ֵ��� | �ܲ��ý��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C12H22O11 | B�� | SO3 | C�� | NaHCO3 | D�� | Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molOH-��1mol-OH������������Ϊ9NA | |
| B�� | 0.1mol/L��CuCl2��Һ�к�Cl-����ĿΪ0.2 NA | |
| C�� | ��״���£�11.2LCCl4�к�C-C������ĿΪ2NA | |
| D�� | 10 mL 2mol/LH2O2��ȫ�ֽ⣬ת�Ƶĵ�����Ϊ0.2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ��״���£�NA ��CO2����ռ�е����Ϊ22.4L | |
| B�� | ���³�ѹ�£�1.06g Na2CO3���е�Na+������Ϊ0.02 NA | |
| C�� | ��״���£�22.4LH2O���еķ�����Ϊ NA | |
| D�� | ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl-����ΪNA |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com