
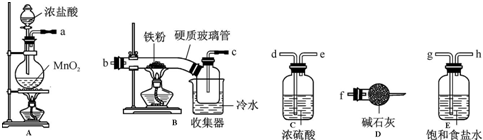
分析 生产无水氯化铁流程:A装置:制取氯气,实验室常用浓盐酸与二氧化锰加热制取MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,制得的氯气中含有HCl和水蒸气,所以先通过E饱和食盐水除HCl,再通C浓硫酸除水蒸气,再通到装置B发生铁和氯气反应2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,最后通入装置D用碱石灰吸收没有反应完的氯气,以防污染空气,同时吸收空气中的水蒸气,防止生成的FeCl3潮解,据此分析解答;
(1)根据排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理分析;
(2)i.根据检查装置的气密性的方法来解答该题;
ii.装置D用碱石灰吸收没有反应完的氯气,以防污染空气,同时吸收空气中的水蒸气,防止生成的FeCl3潮解;
(3)要使沉积的FeCl3进入收集器,根据FeCl3加热易升华的性质;
(5)根据①滴加FeCl3溶液无明显变化,说明SCN-发生了反应而不是Fe3+发生反应,滴加稀HCl和BaCl2溶液,产生白色沉淀,说明生成了硫酸根;
根据②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化,说明O2不能氧化SCN-.
解答 解:(1)浓硫酸具有吸水性能作氯气干燥剂、碱石灰具有碱性而吸收氯气、饱和食盐水吸收氯化氢而抑制氯气溶解,装置排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理,所以装置连接顺序为a→g→h→d→e→b→c→f,故答案为:a、g、h、d、e、b、c、f;
(2)i.根据检查装置的气密性的方法可以知道:把导气管a的一端浸入盛水容器中,用酒精灯轻微加热.若导气管口有气泡冒出,停止加热,在导管内形成一段水柱,则不漏气;故答案为:把导气管a的一端浸入盛水容器中,用酒精灯轻微加热.若导气管口有气泡冒出,停止加热,在导管内形成一段水柱,则不漏气;
ii.根据以上分析,装置D用碱石灰吸收没有反应完的氯气,以防污染空气,同时吸收空气中的水蒸气,防止生成的FeCl3潮解,故答案为:吸收没有反应完的氯气,以防污染空气,同时吸收空气中的水蒸气,防止生成的FeCl3潮解;
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端.要使沉积得FeCl3进入收集器,需进行的操作是对FeCl3加热发生升华使沉积的FeCl3进入收集器,
故答案为:在沉积的FeCl3固体下方加热;
(5)根据①滴加FeCl3溶液无明显变化,说明SCN-发生了反应而不是Fe3+发生反应,滴加稀HCl和BaCl2溶液,产生白色沉淀,说明生成了硫酸根,所以实验①说明SCN-发生了反应而不是Fe3+发生反应;
根据②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化,说明O2不能氧化SCN-,所以氧化SCN-的为双氧水,则实验②的目的是排除H2O2分解产生的O2氧化SCN-的可能;
故答案为:SCN-发生了反应而不是Fe3+发生反应;排除H2O2分解产生的O2氧化SCN-的可能;H2O2将SCN-氧化成SO42-.
点评 本题通过探究氯气与铁反应,考查了物质性质实验方案的设计方法,题目难度稍大,注意掌握氯气与铁反应的现象、反应原理,明确物质性质实验方案的设计原则,试题充分考查了学生的分析、理解能力及化学实验能力.


 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
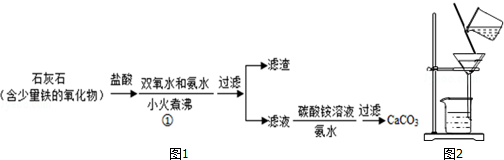
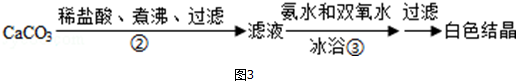
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
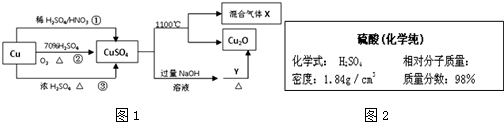
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a气体的相对分子质量一定比b气体的相对分子质量大 | |
| B. | a气体可能是CO,b气体可能是CH4 | |
| C. | A气球中所含气体分子数大于B气球中所含气体分子数 | |
| D. | 充气后,A气球的质量一定大于B气球的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖(C12H22O11) | 25.00 | 342 |
| 硫酸钾 | 0.84 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com