
【题目】 ![]() 和
和![]() 是钍的两种同位素,
是钍的两种同位素,![]() 可以转化成
可以转化成![]() 。下列有关 Th 的说法正确的是( )
。下列有关 Th 的说法正确的是( )
①Th 元素的质量数是 232 ②![]() 和
和![]() 的化学性质相同 ③
的化学性质相同 ③![]() 转换成
转换成![]() 是化学变化 ④Th 元素的相对原子质量是 231 ⑤
是化学变化 ④Th 元素的相对原子质量是 231 ⑤![]() 和
和 ![]() 具有相同的最外层电子数
具有相同的最外层电子数
A.①②B.③④C.②⑤D.④⑤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某小组同学用一种铝铁合金为原料,模拟相关的工业生产,反应过程如图所示(部分产物和条件已略去),请回答:

(1)铁铝合金是一种高电磁性能合金,下列有关推测可能正确的是_____(填序号).
A.铁铝合金可由铁和铝熔融混合制成
B.铁铝合金的熔点高于铝和铁
C.铁铝合金硬度高于纯铝
(2)反应①中铝元素发生反应的离子方程式为_______________________。
(3)反应②的化学方程式为____________________________________。
(4)反应③发生时观察到的现象是_____________________________,用化学方程式表示颜色变化的原因_____________________________________。
(5)反应④中的CO2不宜换成HCl,原因是_____________________。
(6)请举出固体A一种用途_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( )

A. O2在电极b上发生还原反应
B. 溶液中OH-向电极a移动
C. 反应消耗的NH3与O2的物质的量之比为4∶5
D. 负极的电极反应式为2NH3-6e-+6OH-===N2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.是一种重要的有机合成中间体,由芳香烃A和E为有机原料和其他必要试剂制备Ⅰ的合成路线如图:
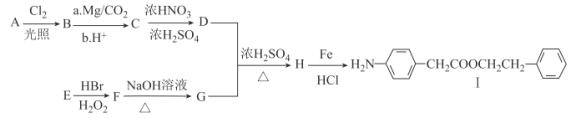
已知:Ⅰ.RX![]() RCOOH;
RCOOH;
Ⅱ.R—CH=CH2![]() R—CH2CH2Br;
R—CH2CH2Br;
Ⅲ.![]() 。
。
请回答下列问题:
(1)A的分子式为___。Ⅰ中含有官能团的名称为_____。
(2)C→D、H→I的反应类型分别为____、____。
(3)E的化学名称为______,一定条件下,E发生加聚反应的化学方程式为____。
(4)F→G的化学方程式为____。
(5)H的结构简式为____。
(6)同时满足下列条件的C的同分异构体有__种(不考虑立体异构);其中核磁共振氢谱有5组峰的结构简式为____。
①能与FeCl3溶液发生显色反应
②能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼元素为人体及动植物必须的微量元素,也在钢铁工业中的有着重要的作用,钼作为钢的合金化元素,可以提高钢的强度,特别是高温强度和韧性。我国钼元素的储量丰富,在世界上占第二位。如图所示是钼元素的相关信息,下列有关钼的说法错误的是

A.95Mo18O42-(钼酸根离子)中共计有 76 个电子
B.95Mo 的相对原子质量是 95.96
C.92Mo、95Mo、98Mo 互为同位素,化学性质几乎相同
D.98Mo 的原子核内有 56 个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)写出元素名称:B_______,G_______。
(2)写出F的价电子排布图:_______。
(3)写出化合物BC的结构式:__________________。
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是________________。
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是______________________。
(6)E的一种晶体结构如图甲,则其一个晶胞中含有_______个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为____pm
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.把在空气中久置的铝片 5.4g 投入盛有 500mL0.5molL-1 盐酸溶液的烧杯中该铝片与盐酸反应产生氢气的速率与反应时间可用如图所示的坐标曲线来表示,回答下列问题:

(1)曲线由 0→a 段不产生氢气的原因______, 用离子方程式表示为______;
(2)曲线由 b→c 段产生氢气的速率增加较快的主要原因______。
(3)向溶液中加入下列物质,能加快上述化学反应速率的是______。
A 蒸馏水 B 改用铝粉 C 饱和氯化钠溶液 D 浓盐酸 E 少量硫酸铜溶液.
Ⅱ.在 2 L 密闭容器中,800 ℃时反应 2NO+O2![]() 2NO2 体系中,n(NO)随时间的变化如下表:
2NO2 体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(4)如图表示各物质浓度的变化曲线,B 点处,v(正)_______v(逆),(用“大于”“小于”或“等于”填空)。

(5)能说明该反应已经达到平衡状态的是______。
a 容器内压强保持不变 b v(NO)=2v(O2)
c 容器内的密度保持不变 d 2v逆(NO2)=v正(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室产生的废液中含有Fe3+、Cu2+、Ba2+三种金属离子,研究小组设计了下列方案对废液进行处理,以回收金属,保护环境。

请回答:
(1)步骤①②④用到的主要玻璃仪器是___________________。
(2)步骤③的实验现象是_________________。
(3) 设计一个实验方案,验证步骤①中所加硫酸溶液己经过量____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1 CH3COOH溶液和HCN溶液,所得滴定曲线如下图。下列说法正确的是

A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B. 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com