
����Ŀ���л���E��C6H8O4���㷺Ӧ����Ϳ����ҵ�У�ijͬѧ�������·�ߺϳ�E������A����Է���������56��B����Է���������A��69����![]()
��1����A�ķ���ʽ�� ��
��2���۵ķ�Ӧ��������Ӧ��
��3����֪EΪ˳ʽ�ṹ�����ýṹ��ʽ��ʾ��ṹ�� ��
��4������˵����ȷ����������ţ���a����Ӧ������ȡ����Ӧ b��B����ȼ��黥Ϊͬϵ��
c��C������������ͬ���칹�� d��D�ܷ������۷�Ӧ
��5����Cת��ΪD��������4����Ӧ��ɣ�C ![]()
![]()
![]()
![]() D�������������Լ�����Ӧ���������ܵĻ�ѧ����ʽ�� ��
D�������������Լ�����Ӧ���������ܵĻ�ѧ����ʽ�� ��
���𰸡�
��1��C4H8
��2��ȡ������������
��3��![]()
��4��ad
��5���������ƴ���Һ�����ȣ�![]()
���������⣺��A����Է���������56����ת����ϵ��C�ķ���ʽC4H8O2��֪��A�����к���4��̼ԭ�ӣ��ʺ�����ԭ����ĿΪ ![]() =8����A�ķ���ʽΪC4H8 �� ��ת����ϵ��֪��BΪ�ȴ�����B����Է���������A��69��BΪ��Ԫ�ȴ�������CΪ��Ԫ������C��D��C4H4O4���ķ���ʽ��֪��C����������Ӧ����D����DΪ��Ԫ���ᣬD�IJ����Ͷ�Ϊ
=8����A�ķ���ʽΪC4H8 �� ��ת����ϵ��֪��BΪ�ȴ�����B����Է���������A��69��BΪ��Ԫ�ȴ�������CΪ��Ԫ������C��D��C4H4O4���ķ���ʽ��֪��C����������Ӧ����D����DΪ��Ԫ���ᣬD�IJ����Ͷ�Ϊ ![]() =3����D�к���C=C˫����D�Ľṹ��ʽΪHOOC��CH=CH��COOH�����ƿ�֪��CΪHOCH2��CH=CH��CH2OH��BΪClCH2��CH=CH��CH2Cl��AΪCH3CH=CHCH3 �� D��CH3OH��Ũ���ᡢ���������·���������Ӧ����E��C6H8O4������E�Ľṹ��ʽΪCH3OOC��CH=CH��COOCH3 �� ��1��������������֪����A�ķ���ʽΪC4H8 �� ���Դ��ǣ�C4H8����2����Ӧ����HOOC��CH=CH��COOH��CH3OH��Ũ���ᡢ���������·���������Ӧ����E��C6H8O4��������ȡ����Ӧ�����Դ��ǣ�ȡ����Ӧ��������Ӧ������3��E�Ľṹ��ʽΪCH3OOC��CH=CH��COOCH3 �� Ϊ˳ʽ�ṹ������ṹΪ��
=3����D�к���C=C˫����D�Ľṹ��ʽΪHOOC��CH=CH��COOH�����ƿ�֪��CΪHOCH2��CH=CH��CH2OH��BΪClCH2��CH=CH��CH2Cl��AΪCH3CH=CHCH3 �� D��CH3OH��Ũ���ᡢ���������·���������Ӧ����E��C6H8O4������E�Ľṹ��ʽΪCH3OOC��CH=CH��COOCH3 �� ��1��������������֪����A�ķ���ʽΪC4H8 �� ���Դ��ǣ�C4H8����2����Ӧ����HOOC��CH=CH��COOH��CH3OH��Ũ���ᡢ���������·���������Ӧ����E��C6H8O4��������ȡ����Ӧ�����Դ��ǣ�ȡ����Ӧ��������Ӧ������3��E�Ľṹ��ʽΪCH3OOC��CH=CH��COOCH3 �� Ϊ˳ʽ�ṹ������ṹΪ�� ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����4��a����Ӧ����CH3CH=CHCH3��������Ӧ����ClCH2��CH=CH��CH2Cl������ȡ����Ӧ����a��ȷ�� b��B�к���C=C˫��������ȼ��鲻��ͬϵ���b���� c��C����������ͬ���칹�壬��CH3CH2CH2COOH�ȣ���c���� d��D�����к���2����COOH���ܷ������۷�Ӧ����d��ȷ�����Դ��ǣ�ad����4��Cת��ΪD��������4����Ӧ��ɣ�C
����4��a����Ӧ����CH3CH=CHCH3��������Ӧ����ClCH2��CH=CH��CH2Cl������ȡ����Ӧ����a��ȷ�� b��B�к���C=C˫��������ȼ��鲻��ͬϵ���b���� c��C����������ͬ���칹�壬��CH3CH2CH2COOH�ȣ���c���� d��D�����к���2����COOH���ܷ������۷�Ӧ����d��ȷ�����Դ��ǣ�ad����4��Cת��ΪD��������4����Ӧ��ɣ�C ![]()
![]()
![]()
![]() D����Ӧ����HCl�����ӳɷ�Ӧ������C=C˫�������Ը��������������Ӧ����ʽΪ��
D����Ӧ����HCl�����ӳɷ�Ӧ������C=C˫�������Ը��������������Ӧ����ʽΪ�� ![]() ����Ӧ�����������ƴ���Һ�����������·�����ȥ��Ӧ����ԭC=C˫�������Դ��ǣ��������ƴ���Һ�����ȣ�
����Ӧ�����������ƴ���Һ�����������·�����ȥ��Ӧ����ԭC=C˫�������Դ��ǣ��������ƴ���Һ�����ȣ� ![]() ��
��


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һֻ��Cl![]() ��CO
��CO![]() ��SO
��SO![]() ��Na
��Na![]() ��K
��K![]() ��Mg
��Mg![]() ���������е�ij���֡���ʵ�飺
���������е�ij���֡���ʵ�飺
��ԭ��Һ![]() ��ɫ������
��ɫ������
��ԭ��Һ�м�BaCl2��Һ������������
��ԭ��Һ�м�AgNO3��Һ������ɫ�������ټ�ϡ�����ɫ�������ܽ⡣�ش��������⣺
��1���Է���ԭ��Һ��һ�����е�������______________��һ�������е�������_______�����ܺ��е�������______________��
��2���е�ͬѧ��Ϊʵ��������ʡ�ԣ�����Ϊ�Ƿ���ȷ��������������������_________��˵������_________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E��F���ֶ�����Ԫ�أ���Ԫ��������Ϣ���£�A�ĵ������ܶ���С�����ʣ�B�ĵ���������ˮ���ҷ�Ӧ������ǿ������Һ�к������ֵ�������ͬ�����������ӣ�C��ԭ�����������������ڲ��������������D��Bͬ���ڣ���������D�ļ����Ӱ뾶��С��B��C��E��ɵ�36���ӵĻ�����Y�Ǽ�������������Ҫ�ɷ֣�FԪ���������������۵Ĵ�����Ϊ4��
��1��д�����־���A��B��C��F����Ԫ�صĻ���������Һ�����Ӧ�����ӷ���ʽ ��
��2��D��E��F�ļ����Ӱ뾶�ɴ�С��˳���ǣ�ֱ���û�ѧʽ��ʾ�� ��
��3����Fe��D������ɵĻ�����У���������F������������Ӧˮ�����ϡ��Һ������ȫ���ܽ⣮�����õ���Һ�м������������������Һ���������ij������˳�������ϴ�ӡ�������պ�õ�һ�ֹ��壬���������ָù����������ԭ����������ǡ����ȣ���ԭ�������D���ʵ���������Ϊ ��
��4��һ������ʯ������ͨ��һ������E���ʣ�����ǡ����ȫ��Ӧ���������������ֺ�EԪ�ص����ӣ������������ӵ����ʵ�����n���뷴Ӧʱ�䣨t����������ͼ��ʾ��t2ʱ��Ӧ�Ļ�ѧ����ʽΪ �� 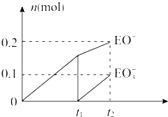
��5��A��B�γɵĻ�����BA���л��ϳ�����;�ܹ㷺�������Զ�ȡ�ܶ�����е����Ӷ�������Ӧ���ƵĻ����д�������Ҵ���Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�������ӷ�Ӧ����( )��
A. ������ԭ����ͭ B. ����ʧȥ�ᾧˮ
C. ����кͷ�Ӧ D. �����������ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D�����ֳ������ʣ����ӦԪ�ص�ԭ���������������ס��ҡ�������Ϊ�������������֮��������ת����ϵ��
�ش��������⣺
��1��A�Ļ�ѧʽΪ���ҵĻ�ѧʽΪ ��
��2��D���Ӧ�Ļ�ѧ����ʽΪ ��
��3��B��NaOH��Һ��Ӧ�����ӷ���ʽΪ �� �÷�Ӧ��������Ϊ ��
��4��B����D�ķ�Ӧ��Ϊ��Ӧ��ʵ�����У����������Ӧ�IJ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̵�ص����С�������������dz��õ�һ�ε�أ��õ�ط�Ӧԭ����ͼ��ʾ�����е����LiClO4���ڻ���л��ܼ��У�����˵����ȷ���ǣ� �� 
A.���·�ĵ�����������a������b��
B.���������ӦʽΪMnO2+e��=MnO ![]()
C.��ϡ��������л��ܼ������������ƶ�������Ũ�ȣ��������ӵ�صĵ���ǿ��
D.Li+ͨ�������Ǩ����MnO2�����У�����LiMnO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ɱ���ܱ�������ʢ��������A��B�Ļ�����壬��һ�������·�����Ӧ��A+3B ![]() 2C��ά���¶Ⱥ�ѹǿ���䣬���ﵽƽ��ʱ�����������ΪV��������C��������ռ10%�������ƶ���ȷ���ǣ� ��
2C��ά���¶Ⱥ�ѹǿ���䣬���ﵽƽ��ʱ�����������ΪV��������C��������ռ10%�������ƶ���ȷ���ǣ� ��
��ԭ�����������Ϊ1.2V����
��ԭ�����������Ϊ1.1V����
�۷�Ӧ��ƽ��ʱ����A���ĵ�0.05V����
�ܷ�Ӧ��ƽ��ʱ����B���ĵ�0.05V����
A.�ڢ�
B.�ڢ�
C.�٢�
D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Pb�Ļ��ϼ�ֻ��+2��+4����+4�۵�Pb����ǿ�����ԣ�������ŨHCl����Cl2��PbO2���ȶ������¶����߰�����˳����PbO2��Pb2O3��Pb3O4��PbO���ֽ�a mol PbO2���ȷֽ⣬�ռ�������O2������Ⱥ����ù����м���������Ũ���ᣬ�ռ�������Cl2 �� ���ȷ�Ӧ�����ù����У�Pb2+ռPbԪ�ص����ʵ�������Ϊx��������Ӧ���ռ���O2��Cl2�����ʵ���֮��Ϊy mol���Իش��������⣺
��1����д��Pb2O3��Ũ���ᷴӦ�Ļ�ѧ����ʽ ��
��2���ú�x��a�ı���ʽ��ʾ������O2��Cl2�����ʵ���n��O2��= �� n��Cl2��= ��
��3��д��y��a��x�ĺ�����ϵʽ�� ��
��4����������Ӧ��O2��Cl2�����ʵ���֮��Ϊ5��3����ʣ������к��е�����Ϊ�������ʵ���֮��Ϊ ��
��5��PbO2��Pb�������������ص�ԭ���ϣ�Ǧ���صĹ���ԭ����Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O������һ������NH4NO3���¹��գ����NO�Ʊ�NH4NO3 �� �乤��ԭ����ͼ��ʾ��Ϊʹ������ȫ��ת��ΪNH4NO3 �� �貹������A��A�� �� ˵�����ɣ� �� ����1�������������Pb�����ʵ�����kg����������������
2PbSO4+2H2O������һ������NH4NO3���¹��գ����NO�Ʊ�NH4NO3 �� �乤��ԭ����ͼ��ʾ��Ϊʹ������ȫ��ת��ΪNH4NO3 �� �貹������A��A�� �� ˵�����ɣ� �� ����1�������������Pb�����ʵ�����kg����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuCl�㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о���ѧϰС�����ȷֽ�ᾧˮ����CuCl��2H2O�Ʊ�CuCl�����������̽����
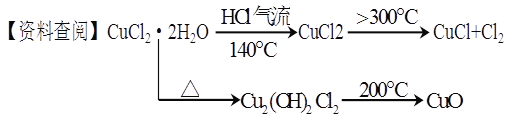
��ʵ��̽������С������ͼ��ʾװ�ý���ʵ�飨�г������ԣ���

��ش��������⣺
��1������X�������� ��
��2��ʵ��������Ⱥ�˳����![]()
![]() ��������ı�ţ���
��������ı�ţ���
a�����װ�õ������Ժ����ҩƷ
b��Ϩ��ƾ��ƣ���ȴ
c�����������������ͨ�����HCl
d����ȼ�ƾ��ƣ�����
e��ֹͣͨ��HCl��Ȼ��ͨ��N2
��3����ʵ������У��۲쵽B�������ɰ�ɫ��Ϊ��ɫ��C����ֽ����ɫ�仯�� ��
��4��װ��D�з�����������ԭ��Ӧ�����ӷ���ʽ�� ��
��̽����˼��
��5����Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʣ�����������Ϣ������
����������CuCl2���������ԭ���� ��
����������CuO���������ԭ���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com