
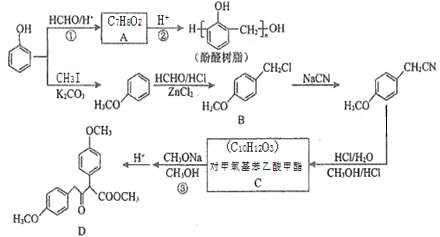
【题目】以甲醛和苯酚为主要原料,经下列转化可合成酚醛树脂和主要的有机合成中间体D(部分反应条件和产物已略去)
已知:R1CH2COOCH3+R2COOCH3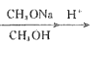 CH3OH+
CH3OH+
请回答下列问题:
(1)C中所含官能团名称为___________;D的化学式为_______。
(2)反应②的化学方程式为_________________。
(3)芳香族化合物E(C8H10O2)与B的水解产物互为同分异构体,1mol E可与2mol NaOH反应,其核磁共振氢谱中有3组峰,且峰面积比为3:1:1,则E有______种可能的结构(不考虑立体异构)。
(4)以CH3OH和CH3ONa为原料(其它试剂任选),设计制备CH3COCH2COOCH3的合成路线:CH3OH![]() ______________。
______________。
【答案】酯基、醚键 C19H20O5 n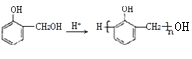 +(n-1)H2O 4 CH3Cl
+(n-1)H2O 4 CH3Cl ![]() CH3CN
CH3CN 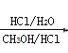 CH3COOCH3
CH3COOCH3![]() CH3COCH2COOCH3
CH3COCH2COOCH3
【解析】
根据题图,①是苯酚和甲醛反应生成A(C7H8O2)的反应,则A为![]() 。C是对甲氧基苯乙酸甲酯,可根据名称写出其结构简式为
。C是对甲氧基苯乙酸甲酯,可根据名称写出其结构简式为![]() 。其余物质的结构简式题目均已给出。
。其余物质的结构简式题目均已给出。
(1)C为![]() ,所含官能团名称为酯基、醚键,D的不饱和度为10,可写出其分子式为C19H20O5;
,所含官能团名称为酯基、醚键,D的不饱和度为10,可写出其分子式为C19H20O5;
(2)②为![]() 发生缩聚反应生成
发生缩聚反应生成![]() 的反应,化学方程式为n
的反应,化学方程式为n![]()
![]()
![]() +(n-1)H2O;
+(n-1)H2O;
(3)B的水解产物为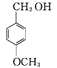 ,1 mol E(C8H10O2)可与2 mol NaOH反应,说明1 mol E 中含有2 mol酚羟基,E的核磁共振氢谱显示有3组峰且峰面积之比为3∶1∶1,则符合条件的E有
,1 mol E(C8H10O2)可与2 mol NaOH反应,说明1 mol E 中含有2 mol酚羟基,E的核磁共振氢谱显示有3组峰且峰面积之比为3∶1∶1,则符合条件的E有![]() 、
、![]() 、
、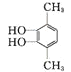 、
、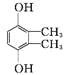 ,共4种;
,共4种;
(4)以CH3OH为原料制备化合物CH3COCH2COOCH3。根据题干中B到D的转化过程,可以首先将CH3OH转化为CH3Cl,再转化为CH3CN,水解再酯化生成乙酸甲酯,最后根据题干信息转化即可。合成路线为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】向一定量的Cu、Fe2O3的混合物中加入400 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
A. 2.4 g B. 3.2 g C. 4.8 g D. 6.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )

A. O3、N2 B. CH4、NH3 C. N2、O2 D. CO、CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.配平__KMnO4 +__HCl=__KCl +__MnCl2 +__Cl2 ↑+__H2O反应方程式,若有1mol氧化剂参加反应,则被氧化的HCl的物质的量___,转移的电子数目___。
II.推理在问题解决过程中常涉及到。同学们要学会从实验数据、物质已知的性质、题给信息等各种渠道收集证据,对物质的性质及其变化提出可能的假设;基于这些证据进行分析推理,最后形成科学结论。
有无色溶液,可能含有K+、SO42-、CO32-、NH4+、Cl-、Ba2+、Cu2+中的一种或几种,按以下步骤进行实验:
①取100ml溶液往其中加入足量稀硫酸,有0.224L(标况下)气体产生;
②另取100ml溶液滴加足量Ba(NO3)2溶液,有4.2g白色沉淀生成;
③继续向②中的溶液滴加足量NaOH溶液并加热,产生刺激性气味的气体0.672L(标况下);根据以上事实判断:
(1)肯定存在的是___。
(2)肯定不存在的是___。
(3)不能确定是否存在的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0mol·L-1的NaOH溶液230mL:
(1)配制溶液时,一般可以分为以下几个步骤:(完成下列空格)
A.计算 B.称量 C.__ D.冷却 E.__ F.__ G.定容 H.摇匀、装瓶
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、量筒、还有___,使用该仪器前必须进行的一步操作是___。
(3)需称量___g烧碱固体,固体应该放在___中称量。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是__。
A.没有洗涤烧杯和玻璃棒
B.转移溶液时不慎有少量洒到容量瓶外面
C.容量瓶不干燥,含有少量蒸馏水
D.定容时俯视刻度线
E.未冷却到室温就将溶液转移到容量瓶并定容
(5)若从所配制溶液取出100mL,再将这100mL溶液加水稀释成1L的溶液,则稀释后所得溶液的物质的量浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值。请回答下列问题:
(1)0.5mol SO2共含有约_______个原子,质量为_______g。
(2)质量相同的①HCl ②NH3 ③CO2 ④O2四种气体中,在同温同压条件下,所占体积最小的是(填序号)___。
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是__________。
(4)0.2 mol NH3分子中所含氢原子数与________个H2O分子中所含氢原子数相等。
(5)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O IO![]() →I2 MnO
→I2 MnO![]() →Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
→Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A. H2O2 B. HNO2 C. MnO![]() D. IO
D. IO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请写出以下溶液的酸碱性(选填“酸性、碱性、中性”)
(1)NaCl溶液______________;
(2)(NH4)2SO4溶液 ___________;
(3)Na2CO3溶液 ___________;
(4)FeCl3溶液 _____________;
(5)CH3COONa溶液 ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各小题。
(1)等浓度的三种溶液①NH4HCO3、② NH4Cl、③NH4HSO4,则c(NH4+)由大到小排列的顺序为____(填序号)。
(2)常温下,将0.1 mol·L-1的HCN溶液和0.1 mol·L-1的NaCN溶液等体积混合,测得混合液中c(HCN)>c(CN-),(假设混合过程中溶液体积的改变忽略不计)。则该混合液pH____7,c(HCN)+c(CN-)_____0.1 mol·L-1,c(HCN)-c(CN-)_____2c(OH-)(填“>”,“<”或“=”)。
(3)小苏打溶液显碱性而不是显酸性的原因:________,溶液中离子浓度大小顺序:___________。
(4)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
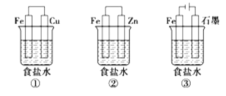
为防止金属Fe被腐蚀,可以采用上述________装置(填装置序号)原理进行防护;装置③中总反应的离子方程式为____________________。检验石墨电极产物气体的方法:_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com