
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:

下列叙述正确的是( )。
A. X、Y和Z均能使溴水褪色,且原理相同
B. X和Z均能与Na2CO3溶液反应放出CO2
C. X、Y和Z分子中的所有原子可能共平面
D. X苯环上一氯代物有3种,Y苯环上的二氯代物有6种
科目:高中化学 来源: 题型:
【题目】我国科学家发明了一种“可固氮”的锂-氮二次电池,将可传递![]() 的醚类作电解质,电池的总反应为6Li +N2
的醚类作电解质,电池的总反应为6Li +N2![]() 2Ll3N,下列说法不正确的是( )
2Ll3N,下列说法不正确的是( )

A.固氮时,阳极区发生反应![]()
B.脱氮时,钌复合电极的电极反应:![]()
C.醚类电解质可换成![]() 溶液
溶液
D.脱氮时,![]() 向锂电极迁移
向锂电极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象与实验操作不相匹配的是( )
实验操作 | 实验现象 | |
A | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
B | 向盛有高锰酸钾酸性溶液的试管中通入足 量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究![]() 和
和![]() 的反应规律。实验操作及现象如下:
的反应规律。实验操作及现象如下:
实验及试剂 | 编号 | 无色 | 试管中溶液颜色 | 淀粉KI试剂颜色 |
| 1 | 0.5mL | 浅黄色 | 无色 |
2 | 0.20mL | 深黄色 | 无色 | |
3 | 0.25mL | 浅黄色 | 蓝色 | |
4 | 0.30mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如下实验:

经康康同学检验,上述白色沉淀是![]() 。写出加入0.20mL
。写出加入0.20mL ![]() 后,溶液中
后,溶液中![]() 和
和![]() 发生反应的离子方程式:____________。
发生反应的离子方程式:____________。
(2)查阅资料:一定条件下,![]() 和
和![]() 都可以被氧化成
都可以被氧化成![]() 。
。
作出假设:![]() 溶液用量增加导致溶液褪色的原因是过量的
溶液用量增加导致溶液褪色的原因是过量的![]() 溶液与(1)中的反应产物继续反应,同时生成
溶液与(1)中的反应产物继续反应,同时生成![]() 。进行实验:
。进行实验:
①取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有![]() 。
。

其中试剂X可以是_________(填字母序号)。
a 碘水 b ![]() 溶液 c
溶液 c ![]() 溶液 d
溶液 d ![]() 溶液
溶液
②李政同学提出,仅通过润湿淀粉![]() 试纸变蓝的现象不能说明生成
试纸变蓝的现象不能说明生成![]() ,理由是_______,便补充了如下实验:将实验4中的湿润淀粉
,理由是_______,便补充了如下实验:将实验4中的湿润淀粉![]() 试纸替换为________,在滴加
试纸替换为________,在滴加![]() 溶液后,发现________,进一步佐证实验4中生成了
溶液后,发现________,进一步佐证实验4中生成了![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是
A. HCO3的电离方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. 泡沫灭火器的原理:Al3++3HCO3- ![]() Al(OH)3↓+3CO2↑
Al(OH)3↓+3CO2↑
C. NH4Cl溶于D2O中:NH4++D2O![]() NH3·D2O+H+
NH3·D2O+H+
D. Na2S显碱性原因:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式为 ,下列有关该化合物的叙述不正确的是
,下列有关该化合物的叙述不正确的是
A.该有机物的分子式为C11H12O2
B.1mol该物质最多能与4molH2发生反应
C.该有机物分子中所有原子一定在同一个平面上
D.该有机物一定条件下,可以发生取代、加成、氧化、酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中说法不正确的是( )
A.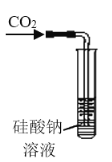 可用来证明碳的非金属性比硅强
可用来证明碳的非金属性比硅强
B.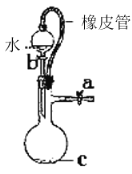 橡皮管的作用是能使水顺利流下
橡皮管的作用是能使水顺利流下
C. 用图示的方法不能检查此装置的气密性
用图示的方法不能检查此装置的气密性
D. 先从①口进气集满CO2,再从②口进气,可收集NO
先从①口进气集满CO2,再从②口进气,可收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O) ,流程如下:
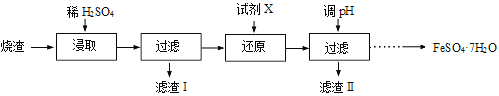
(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为 。能提高烧渣浸取速率的措施有 (填字母)。
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
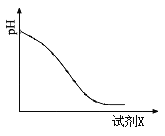
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是 (填字母)。
A.Fe粉 B.SO2 C.NaI
还原结束时,溶液中的主要阴离子有 。
(3)滤渣Ⅱ主要成分的化学式为 ;由分离出滤渣Ⅱ后的溶液得到产品,进行的操作是 、 过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组对NaOH溶液和稀盐酸混合后的有关问题进行了如下探究:查阅资料:下表是实验室里盐酸、NaOH试剂瓶标签上的部分说明:

实验探究:
(1)配制溶液:甲同学配制100 mL 1.5 mol·L-1NaOH溶液,乙同学取20 mL 36.5%的盐酸稀释到200 mL。甲为了证明NaOH溶液与稀盐酸能发生化学反应,设计并完成了如下图所示的实验。

X溶液滴入的量一般为______,使用酸式滴定管前要检查活塞是否漏水的操作方法是________。
(2)乙设计完成了另一个实验,以证明NaOH溶液与盐酸能够发生反应。他在盛有20 mL稀盐酸的锥形瓶里,用碱式滴定管滴入NaOH溶液,不断振荡溶液,同时用pH计测定溶液的pH,直到NaOH溶液过量。则在滴定过程中,滴定终点附近的操作是_______。
(3)你认为甲、乙两位同学的实验中,______(填“甲”、“乙”或“甲和乙”)的实验能充分证明NaOH与盐酸发生了反应。
(4)丙同学为了测定上述36.5%盐酸的物质的量浓度,进行了如下实验:在锥形瓶中加入已稀释的盐酸,用碱式滴定管滴入甲配制的NaOH溶液,测定的结果如下表:

据此通过计算可知实验测定的盐酸浓度与标签说明的浓度相比_____(填“偏高”、“偏低”或“相等”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com