
【题目】下列气体去除杂质的方法中,不能实现目的的是
气体(杂质) | 方法 | |
A | SO2(H2S) | 通过酸性高锰酸钾溶液 |
B | Cl2(HCl) | 通过饱和的食盐水 |
C | N2(O2) | 通过灼热的铜丝网 |
D | NO(NO2) | 通过氢氧化钠溶液 |
A.AB.BC.CD.D
【答案】A
【解析】
A.SO2和H2S都具有较强的还原性,都可以被酸性高锰酸钾溶液氧化;因此在用酸性高锰酸钾溶液除杂质H2S时,SO2也会被吸收,故A项不能实现除杂目的;
B.氯气中混有少量的氯化氢气体,可以用饱和食盐水除去;饱和食盐水在吸收氯化氢气体的同时,也会抑制氯气在水中的溶解,故B项能实现除杂目的;
C.氮气中混有少量氧气,在通过灼热的铜丝网时,氧气可以与之发生反应:![]() ,而铜与氮气无法反应,因此可以采取这种方式除去杂质氧气,故C项能实现除杂目的;
,而铜与氮气无法反应,因此可以采取这种方式除去杂质氧气,故C项能实现除杂目的;
D.NO2可以与NaOH发生反应:![]() ,NO与NaOH溶液不能发生反应;尽管NO可以与NO2一同跟NaOH发生反应:
,NO与NaOH溶液不能发生反应;尽管NO可以与NO2一同跟NaOH发生反应:![]() ,但由于杂质的含量一般较少,所以也不会对NO的量产生较大的影响,故D项能实现除杂的目的;
,但由于杂质的含量一般较少,所以也不会对NO的量产生较大的影响,故D项能实现除杂的目的;
答案选A。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
【题目】向盛有Cl2的三个集气瓶甲、乙、丙中各注入下列液体中的一种,经过振荡,现象如下图所示,则甲、乙、丙中注入的液体分别是( )

A. ①②③ B. ③②① C. ②①③ D. ①③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某恒容密闭容器中加入1.6 mol L-1的NO2后,会发生如下反应:2NO2(g)N2O4(g) △H =-56.9kJmol-1。其中N2O4的物质的量浓度随时间的变化如图所示,下列说法不正确的是

A.升高温度,60s后容器中混合气体颜色加深
B.0-60s内,NO2的转化率为75%
C.0-60s内,v(NO2)=0.02mol L-1 s-1
D.a、b两时刻生成NO2的速率v(a)>v(b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气的流程如下。
![]()
请回答下列问题:
Ⅰ.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。
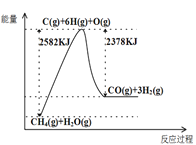
(1)该过程的热化学方程式是__________。
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1_______T2(填“>”“<”或“=”),并说明理由__________。

(3)一定温度下,在1L恒容的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为______________。
Ⅱ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅲ.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下:
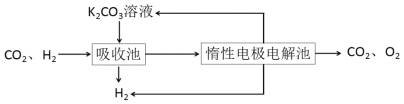
依据图示信息回答:
(4)吸收池中发生反应的离子方程式是_________。
(5)写出电解池中阳极发生的电极反应式________;结合化学用语说明K2CO3溶液再生的原因_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。


(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是 ______________________。
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色。为测定该实验所得 “铁块”中铁元素含量,设计实验流程如图所示。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
Fe2+ | Fe3+ | Al3+ | Mg2+ | |
开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
① 试剂A应选择________,试剂B应选择_______。(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
② 写出反应Ⅱ的离子方程式_____________________。
③ 设计简单实验证明M的成分是Fe2O3而非Fe3O4。
操作 | 预期现象 |
取少量M固体于试管中,向其中加入________________;观察。 | 固体完全溶解,溶液呈黄色。 |
继续向上述溶液中滴入_________________,振荡观察 | ______________________ |
④ 上述实验应灼烧至M质量不变,则能证明M质量不变的标志是____________。
⑤ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
i.CO(g)+2H2(g)![]() CH3OH(g) H1=90.1kJ·mol1
CH3OH(g) H1=90.1kJ·mol1
ii.2CH3OH(g)![]() CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X 的变化曲线如右图所示。下列说法正确的是
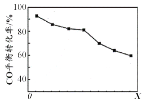
A . 由H2和CO直接制备二甲醚的反应为放热反应
B. 条件X为压强
C. X增大,二甲醚的产率一定增大
D. X增大,该反应的平衡常数一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家近年发明了一种新型ZnCO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
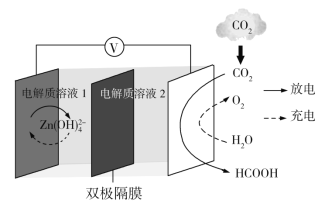
下列说法错误的是
A.放电时,负极反应为![]()
B.放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol
C.充电时,电池总反应为![]()
D.充电时,正极溶液中OH浓度升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电致变色器件可智能调控太阳光透过率,从而实现节能。下图是某电致变色器件的示意图。当通电时,Ag+注入到无色WO3薄膜中,生成AgxWO3,器件呈现蓝色,对于该变化过程,下列叙述错误的是
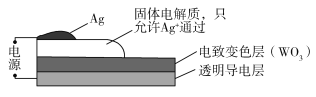
A.Ag为阳极B.Ag+由银电极向变色层迁移
C.W元素的化合价升高D.总反应为:WO3+xAg=AgxWO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了减少“84”消毒液对物品的腐蚀,天津一中高三师生给教室消毒使用的是二氧化氯泡腾片。二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体 ,其熔点为 -59℃,沸点为11.0℃,易溶于水。是目前国际上公认的新—代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面有广泛应用的高效安全消毒剂。与(Cl2)相比(ClO2)不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
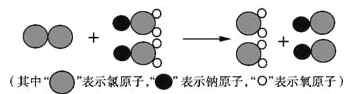
该反应的化学方程式为 ____________。
Ⅰ.ClO2是—种优良的消毒剂 ,浓度过高时易发生分解,为了运输和贮存便利常将其制成NaClO2固体 ,模拟工业上用过氧化氢法制备NaClO2固体的实验装置如图所示:
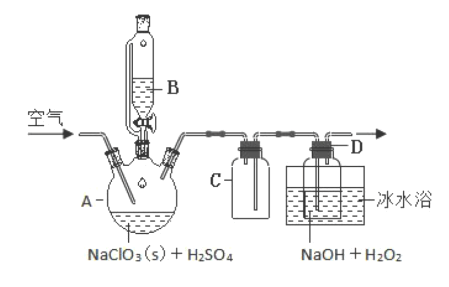
已知:H2O2沸点 150℃;A中的化学方程式:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(2)NaClO3放入仪器 A中,仪器B中的药品是________(写化学式)。
(3)如果仪器B 改成分液漏斗,实验过程中可能会出现的实验现象_______。
(4)向 A 装詈中通入空气,其作用是赶出ClO2然后通过C 再到 D 中反应。通空气不能过快的,空气流速过快时ClO2不能被充分吸收;通空气也不能过慢,其原因是_________。
(5)冰水浴冷却的目的是_____。
a.降低NaClO2的溶解度 b.减少H2O2的分解
c.使ClO2变为液态 d. 加快反应速率
Ⅱ.“稳定性二氧化氯溶液”是淡黄色透明液体,广泛应用于食品卫生等领域的杀菌消毒。ClO2稳定性较差,“稳定性二氧化氯溶液”是以碳酸钠为稳定剂,有效成分为NaClO2。
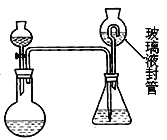
某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题:
(6)为证实“稳定性二氧化氯溶液”中含有钠离子,方法是:______。
(7)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取 mg(2g 左右)试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液 ;②在锥形瓶中加入4g 碘化钾,用 100 mL水溶解后 ,再加 3 mL 硫酸溶液 ;③ 在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmo l/L硫代硫酸钠标准溶液滴定至蓝色消失 (![]() ), 共用去VmL 硫代硫酸钠溶液。
), 共用去VmL 硫代硫酸钠溶液。
①NaClO2与盐酸反应生成ClO2(还原产物为Cl-)该反应的化学方程式为:_______;
②ClO2通入锥形瓶与酸性碘化钾溶液反应,二氧化氯被还原为氯离子,该反应的离子方程式为:_______。
③“稳定性二氧化氯溶液”中,ClO2的质量分数为_____(用m、c、V表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com