
【题目】下列实验设计方案一定可行的是( )
A. 用水鉴别苯和四氯化碳B. 用蒸发结晶的方法除去KNO3中混有少量的NaCl
C. 用分液的方法分离碘的四氯化碳溶液D. 用酒精萃取碘水中的碘
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 1 mol CH4的质量为16g/mol
B. CH4的摩尔质量为16g
C. 标准状况下,O2的摩尔体积约为22.4L/mol
D. 标准状况下,1 mol H2O的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某100 mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.4 mol·L-1和0.4 mol·L-1。向该混合溶液中加入1.92 g铜粉,加热,待充分反应后(假设反应前 后溶液体积不变),所得溶液中Cu2+的物质的量浓度是( )
A. 0.15 mol·L-1 B. 0.225 mol·L-1
C. 0.30 mol·L-1 D. 0.45 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验操作的说法中正确的是
A. 分液时,下层液体从下口放出,上层液体从上口倒出
B. 蒸发时,应使混合物中的水分完全蒸干后,再停止加热
C. 蒸馏时,温度计的水银球插入液面以下
D. 用100mL量简量取8.5mL浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生产和生活中有着广泛的应用. I.氧化铁是重要工业颜料,用废铁屑制备它的流程如图: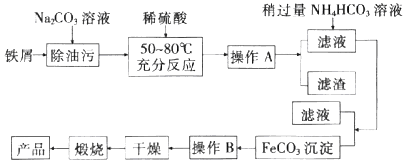
回答下列问题:
(1)操作A、B的名称分别是、;加入稍过量的NH4HCO3溶液的作用是 .
(2)写出在空气中充分加热煅烧FeCO3的化学方程式: .
(3)II.上述流程中,若煅烧不充分,最终产品中会含有少量的FeO杂质.某同学为测定产品中Fe2O3的含量,进行如下实验: a.称取样品8.00g,加入足量稀H2SO4溶解,并加水稀杯至100mL;
b.量取25.00mL待测溶液于锥形瓶中;
c.用酸化的0.01000molL﹣1KMnO4标准液滴定至终点;
d.重复操作b、c2~3次,得出消耗KMnO4溶液体积的平均值为20.00mL.
写出滴定过程中发生反应的离子方程式: .
(4)确定滴定达到终点的操作及现象为 .
(5)上述样品的质量分数为 .
(6)下列操作会导致样品中Fe2O3的质量分数的测定结果偏低的有 . a.未干澡锥形瓶 b.盛装标准液的滴定管没有用标准液润洗
c.滴定结束时仰视刻度线读数 d.量取待测液的滴定管没有润洗.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】屠呦呦因对青蒿素的研究而获得诺贝尔生理学或医学奖,青蒿素可以青蒿酸(结构简式如图所示)为原料合成,下列关于青蒿酸的说法中正确的是( ) 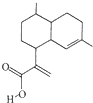
A.分子式为C15H24O2
B.属子芳香族化合物
C.能发生取代反应和加成反应
D.分子中所有原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应aA(g)+bB(g)cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系: ![]() =K(为一常数),K称为化学平衡常数,其反应的K值只与温度有关.现有反应:CO(g)+H2O (g)CO2(g)+H2(g)△H<0.在850℃时,K=1.
=K(为一常数),K称为化学平衡常数,其反应的K值只与温度有关.现有反应:CO(g)+H2O (g)CO2(g)+H2(g)△H<0.在850℃时,K=1.
(1)若升高温度到950℃时,达到平衡时K1(填“大于”“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和x mol H2 , 则:
①当x=5.0时,上述平衡向(填“正反应”或“逆反应”)方向移动.
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】清洁能源具有广阔的开发和应用前景,可减少污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池.一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)CH3OH(g)△H=﹣105kJmol﹣1 . 向体积为2L的密闭容器中充入2molCO和4molH2 , 测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示: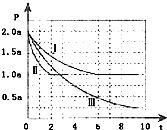
(1)Ⅱ和Ⅰ相比,改变的反应条件是 .
(2)反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)= .
(3)反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)= .
(4)比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1T3(填“>”“<”“=”),判断的理由是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com