
【题目】水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.请回答下列问题:
(1)天然水中溶解的气体主要有___________、___________;
(2)天然水在净化处理过程中加入的混凝剂可以是___________,其纯净水作用的原理是___________;
(3)水的纯净和软化的区别是___________;
(4)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO).若某天然水中c(Ca2+)=1.2×10-3molL-1,c(Mg2+)=6×10-4molL-1,则此水的硬度为___________;
(5)若(4)中的天然水还含有c(HCO3-1)=8×10-4molL-1,现要软化10m3这种天然水,则需先加入Ca(OH)2 ___________g,后加入Na2CO3 ___________g。
【答案】(1)O2;CO2(或氮气)
(2)明矾、硫酸铝、硫酸铁、硫酸亚铁
铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,它可吸附天然水中悬浮物并破坏天然水中的其他带异电的胶体,使其聚沉,达到净化目的
(3)水的净化是用混凝剂(如明矾等)将水中胶体及悬浮物沉淀下来,而水的软化是除去水中的钙离子和镁离子
(4)10°
(5)740;1484
【解析】
试题分析:(1)氧气能够较少量地溶解在水中,二氧化碳能够较多量地溶解在水中,所以天然水中溶解的气体主要有氧气和二氧化碳,故答案为:O2;CO2(或氮气);
(2)混凝剂是吸附水中的微小悬浮颗粒,凝聚成较大的颗粒,而快速沉降的主要作用,要具备水解生成胶体的性质,所以常有铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,如明矾、硫酸铝、硫酸铁、硫酸亚铁等,故答案为:明矾、硫酸铝、硫酸铁、硫酸亚铁;铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,它可吸附天然水中悬浮物并破坏天然水中的其他带异电的胶体,使其聚沉,达到净化目的;
(3)水的净化是除去悬浮性杂质,一般用明矾进行;水的软化是降低Ca2+、Mg2+的浓度,方法很多,有离子交换法、石灰纯碱法等,故答案为:水的净化是用混凝剂(如明矾等)将水中胶体及悬浮物沉淀下来,而水的软化是除去水中的钙离子和镁离子;
(4)某天然水中c(Ca2+)=1.2×10-3molL-1,c(Mg2+)=6×10-4molL-1,硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO);1L水中钙离子物质的量=1.2×10-3mol,相当于CaO质量=1.2×10-3mol×56g/mol=67.2mg,1L水中镁离子物质的量=6×10-4mol,相当于氧化镁质量6×10-4mol×40g/mol=24mg,所以水的硬度=![]() +
+![]() =10°故答案为:10°;
=10°故答案为:10°;
(5)10m3这种天然水水中含有钙离子物质的量=10×103L×1.2×10-3molL-1=12mol;镁离子物质的量=10×103L×6×10-4molL-1=6mol;碳酸氢根离子物质的量=10×103L×8×10-4molL-1=8mol;加入氢氧化钙发生的反应为:
Mg2++2OH-=Mg(OH)2↓ HCO3-+OH-=CO32-+H2O
1 2 1 1 1
6mol 12mol 8mol 8mol 8mol
共需氢氧根物质的量20mol;需要Ca(OH)2物质的量10mol,氢氧化钙质量为74g/mol×10mol=740g,水溶液中Ca2+物质的量为12mol+10mol=22mol,其中需要加入的 碳酸根离子为22mol-8mol=14mol,需要碳酸钠的质量为14mol×106g/mol=1484g,故答案为:740;1484。


科目:高中化学 来源: 题型:
【题目】I、下列七种有机物中:
①CH4
②CH2=CH2
③![]()
④CH3COOH
⑤HOCH2CHO
⑥CH3CH2CH2CH3
⑦葡萄糖
⑧蛋白质
⑨淀粉
(1)可与浓硝酸发生颜色反应的是______________(填序号,下同)。
(2)属于同系物的是 。
(3)互为同分异构体的是___________。
(4)易发生银镜反应的是______________。
II、在5L的密闭容器中充入1mol A 和2mol B,在一定条件下发生反应4A(g)+5B(g)![]() 4C(g)+6D(g),半分钟后,C的物质的量增加了0.30mol。
4C(g)+6D(g),半分钟后,C的物质的量增加了0.30mol。
(5)D的平均反应速率为 。
(6)A的转化率为 。
(7) 不能判断该反应已达平衡状态的是 。
A .单位时间内生成n mol A的同时生成2n mol D的状态
B .生成物浓度不再变化的状态
C .混合气体的平均相对分子质量不再改变的状态
D .混合气体的压强不再改变的状态
E. 容器中各组分的体积分数不随时间变化的状态
F .容器中A、B、C、D的物质的量的比一定是4:5:4:6的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. 温度越高,酶的催化活性越强
B. 浓硝酸使皮肤呈黄色是由于浓硝酸与蛋白质发生了颜色反应
C. 用灼烧的方法可以鉴别毛织物和棉织物
D. 在豆浆中加入少量的石膏,能使豆浆凝结为豆腐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质性质与应用对应关系正确的是( )
A.浓硫酸具有吸水性,可用于干燥CO2
B.硅有导电性,可用作光导纤维
C.铝具有高熔点,可用于生产耐火砖
D.氨气具有还原性,可用于检查HCl泄漏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关性质的比较,能用元素周期律解释的是
A. 酸性:HC1>H2S B. 单质活泼性:Sn>Pb
C. 碱性:Na2SiO3>Na2CO3 D. 沸点:NH3>PH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
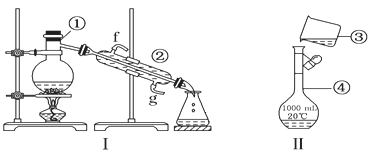
(1)写出下列仪器的名称:
①___________;②___________;④___________;
(2)仪器①~④中,使用时必须检查是否漏水的有___________(填序号)
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器有___________,将仪器补充完整后进行的实验操作的名称为___________;②的进水口是___________(填f或g)
(4)现需配制250ml 0.2mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误操作___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为___________ ,W3分子的空间结构为___________;
(2)X单质与水发生主要反应的方程为___________;
(3)化合物M的化学式为___________,其晶体结构与NaCl相同,而熔点高于NaCl.M熔点较高的原因是___________,将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯.在碳酸二甲酯分子中,碳原子采用的杂化方式有___________ ,O-C-O的键角约为___________;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成X:Y:Z= ___________;
(5)许多金属盐都可以发生焰色反应,其原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 ⑴已知碳酸二级电离较偏铝酸的电离容易,而石炭酸的电离介于碳酸的一级电离与二级电离之间。下面的推论正确的是_________________:
①将CO2通入偏铝酸钠溶液中,溶液变浑浊,并生成碳酸钠或碳酸氢钠;②将CO2通入C6H5ONa溶液中,离子反应式为CO2+H2O+2C6H5O—![]() 2 C6H5OH+CO32—;
2 C6H5OH+CO32—;
③HCO3—在溶液中既能与AlO2—又能与Al3+反应,且都发生双水解;④往含有大量CO32—的溶液中加入C6H5OH得到澄清溶液,放出CO2气体;⑤向Al(OH)3的混浊液中加入Na2CO3溶液得不到澄清溶液;⑥相同温度,相同浓度的Na2CO3、C6H5ONa、NaHCO3、NaAlO2的稀溶液PH依次增大。
(2)浅绿色的Fe(NO3)2溶液中,存在如下平衡:Fe2++2H2O![]() Fe(OH) 2+2H+若在此溶液中加入盐酸后,用文字说明溶液颜色的变化及原因__________________.
Fe(OH) 2+2H+若在此溶液中加入盐酸后,用文字说明溶液颜色的变化及原因__________________.
⑶一个完整的氧化还原反应方程式可以拆开,写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-=Cu2+,还原反应式:2Fe3++2e-=2Fe2+。据此,回答下列问题:
①将反应3 Cu+8H+ +2NO3-=3Cu2++2NO↑+4H2O拆写为两个“半反应式”:
还原反应式: 。
②已知某反应的两个“半反应式”为:
CH4+10 OH--8e-=CO32-+7H2O, O2+2H2O+4e-= 4OH-,
则氧化还原反应方程式为 。
③此原理可用于电化学。锌—锰碱性电池广泛应用于日常生活。电池的总反应式为Zn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)。
该电池的正极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com