
分析 A是周期表中原子半径最小的元素,应为H元素;B元素的最高价氧化物的水化物与其氢化物能相互反应生成盐,应为N元素;A元素与C元素可形成两种液态化合物,其分子中电子总数分别为10和18,形成的化合物为H2O和H2O2,则C为O元素;D元素的主族序数等于其周期数,应为Al元素;E元素原子的最外层电子数是其电子层数的2倍,应为S元素,结合元素对应单质、化合物的性质以及在周期表中的位置解答该题.
解答 解:A是周期表中原子半径最小的元素,应为H元素;B元素的最高价氧化物的水化物与其氢化物能相互反应生成盐,应为N元素;A元素与C元素可形成两种液态化合物,其分子中电子总数分别为10和18,形成的化合物为H2O和H2O2,则C为O元素;D元素的主族序数等于其周期数,应为Al元素;E元素原子的最外层电子数是其电子层数的2倍,应为S元素,
(1)E为S元素,原子序数为16,核外有3个电子层,最外层电子数为6,应位于周期表第三周期第VIA族,
故答案为:第三周期第 VIA族;
(2)A与C形成的18电子物质为H2O2,含H-O极性共价键、O-O非极性共价键,则所含的化学键类型是BC,
故答案为:BC;
(3)A和E形成的化合物为二元弱酸,分步电离,以第一步为主,则在水中的电离方程式H2S?H++HS-,
故答案为:H2S?H++HS-;
(4)制备D的最高价氧化物的水化物的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(5)N元素与O元素形成的化合物中相对分子质量最小的是NO,与氧气按物质的量之比为4:1反应,发生反应为4NO+O2+4NaOH=4NaNO2+2H2O,故答案为:NaNO2.
点评 本题考查位置、结构、性质的关系及应用,为高频考点,推断元素为解答的关键,侧重分析与推断及元素化合物知识的综合考查,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 转移0.1mol电子时,a电极产生1.12LH2 | |
| B. | b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- | |
| C. | c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池 | |
| D. | d电极上发生的电极反应是:O2+4H++4e-=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都可以保存在煤油中 | B. | 随电子层数增加,熔沸点逐渐降低 | ||
| C. | 都是银白色金属,质软,有延展性 | D. | 随电子层数增加,密度逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
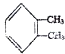 ;若C8H10分子中苯环上的一氯代物有三种,则其结构简式为
;若C8H10分子中苯环上的一氯代物有三种,则其结构简式为 或
或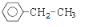 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加热 | B. | 加入少量CaO(s) | C. | 加入少量NaOH(s) | D. | 加入少量CaCl2(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z | B. | 单质的非金属性:X>Y>Z | ||
| C. | 气态氢化物稳定性:X>Y>Z | D. | 原子序数:X>Y>Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com