
 Ϊ���ѧѧ����ȡ�õijɾ��Լ������������Ĺ��ף����Ϲ���2011�궨Ϊ�����ʻ�ѧ�ꡱ��������Ϊ����ѧ�������ǵ�������ǵ�δ��������ѧ��עʳƷ��ȫ�����ཡ�������Ŀɳ�����չ��Ϊ�����������������������������ˮƽ��������Ҫ���ã���ش��������⣺
Ϊ���ѧѧ����ȡ�õijɾ��Լ������������Ĺ��ף����Ϲ���2011�궨Ϊ�����ʻ�ѧ�ꡱ��������Ϊ����ѧ�������ǵ�������ǵ�δ��������ѧ��עʳƷ��ȫ�����ཡ�������Ŀɳ�����չ��Ϊ�����������������������������ˮƽ��������Ҫ���ã���ش��������⣺���� ��1��ά���ؼȲ����빹������ϸ����Ҳ��Ϊ�����ṩ���������������������Ҫ����С������������ĸ������������Ҫ�����ã��������ȱ��ά����A�Ỽҹä֢��ȱά����C�Ỽ��Ѫ�����ֿ����½���ȱά����D�Ỽ���Ͳ����������ɣ��ݴ˽��
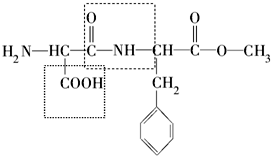
��2�����ݰ�˾����Ľṹ��ʽ�����жϰ�˾������������߿��ڹ����ŵ�����Ϊ�ļ����Ȼ���
��3��ȱ�������ʻ�Ӫ��ȱ��֢������ʳ���к��е����ʣ�
��4��ΪԤ����ȱ������������ʳ��������KIO3��ΪӪ��ǿ���������⣻̼���������ȷֽ����ɶ�����̼���������Ϊ���ɼ���
��5���ֽ���������ڸ��ϲ��ϣ������������ǽ������ϣ����첣������Ҫԭ��Ϊ���ʯ��ʯ��ʯӢ����������е�����������Ӧ�����������һ�����ܵ�����Ĥ��������һ������ʴ�����ά����Ҫ�ɷ���SiO2��
��� �⣺��1���ܷ���ҹä֢����ά����A����Ԥ�����Ͳ�����ά����D���ܷ��λ�Ѫ������ά����C���ʴ�Ϊ���ܣ��٣�
��2���ɰ�˾����Ľṹ��ʽ����˾������������߿��ڹ����ŵ�����Ϊ�ļ����Ȼ����ʴ�Ϊ���ļ����Ȼ���
��3��ȱ�������ʻᵼ���������������ϰ�����Ӫ��ȱ��֢������ʳ���и��������ʣ����������к��зḻ�ĵ����ʣ�
�ʴ�Ϊ�������ʣ�C��
��4��ΪԤ����ȱ������������ʳ��������KIO3��ΪӪ��ǿ���������⣻̼���������ȷֽ����ɶ�����̼���������Ϊ���ɼ�������ʽΪ��2NaHCO3 $\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2�����ʴ�Ϊ��KIO3��2NaHCO3 $\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
��5���ֽ���������ڸ��ϲ��ϣ������������ǽ������ϣ����첣������Ҫԭ��Ϊ���ʯ��ʯ��ʯӢ����Ϊ��������е�����������Ӧ�����������һ�����ܵ�����Ĥ��������һ������ʴ���������ڿ�����ȴ�������ֳ����õĿ���ʴ�ԣ����ά����Ҫ�ɷ���SiO2��
�ʴ�Ϊ�����ϲ��ϣ����ǽ����������������е�����������Ӧ�����������һ�����ܵ�����Ĥ��SiO2��
���� ���⿼���Ϊ�ۺϣ�������Ӫ�����ʡ������Լ�ҽҩ�ȽǶȵĿ��飬Ϊ�߿��������ͣ�����������ѧ�������õĿ�ѧ���������ѧϰ�Ļ����ԣ��ѶȲ���ע�⻯ѧ�������������е�ʵ��Ӧ�����ص㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��SiO2��CO��Ϊ���������� | B�� | ϡ���������ᡢ�Ȼ�����Һ��Ϊ���� | ||
| C�� | ���ᡢˮ��������ˮ��Ϊ����� | D�� | �ռ�����ᡢ���Ȼ�̼��Ϊ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

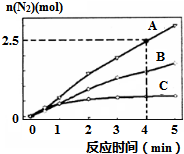
| ��� | ��Ӧ�¶�/�� | Na2S2O3ŨҺ/mL | �� | 0.1mol/LH2SO4��Һ/mL | �� |
| �� | 25�� | 10.0 | 0 | 10.0 | |
| �� | 25�� | 5.0 | a | 10.0 | |
| �� | 45�� | 10.0 | 0 | 10.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | ���볣����25�棩 |
| HCN | K=4.9��10-10 |
| CH3COOH | K=1.8��10-5 |
| H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ��������������������й㷺��;��
��������������������й㷺��;���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������O2-+2H+�TH2O | |
| B�� | �����ʯ��ˮ��ͨ�������CO2��Ca2++2OH-+CO2�TCaCO3��+H2O | |
| C�� | ����ʯ��ˮ��Ca��HCO3��2��Һ��Ӧ��Ca2++HCO3-+OH-�TCaCO3��+H2O | |
| D�� | ����������Һ������þ��Һ��Ӧ��Ba2++SO42-�TBaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
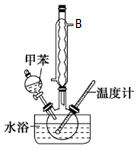 �����ױ����졢�䡢�����֣����ж������ױ���ҽҩ��Ⱦ�ϵȹ�ҵ��һ����Ҫ�л��м��壬������Ũ����Ϊ��������Ũ����Ϊ������ͨ���ױ���������Ӧ�Ʊ���һ���µ��Ʊ��������ױ���ʵ�鷽���ǣ��Է�������Ϊ������������NaHSO4Ϊ��������ѭ��ʹ�ã�����CCl4��Һ�У�����������������ˮ���ã���45�淴Ӧ1h����Ӧ�������ˣ���Һ�ֱ���5%NaHCO3����Һ��ˮϴ�����ԣ��پ������ᴿ�õ��������ױ���
�����ױ����졢�䡢�����֣����ж������ױ���ҽҩ��Ⱦ�ϵȹ�ҵ��һ����Ҫ�л��м��壬������Ũ����Ϊ��������Ũ����Ϊ������ͨ���ױ���������Ӧ�Ʊ���һ���µ��Ʊ��������ױ���ʵ�鷽���ǣ��Է�������Ϊ������������NaHSO4Ϊ��������ѭ��ʹ�ã�����CCl4��Һ�У�����������������ˮ���ã���45�淴Ӧ1h����Ӧ�������ˣ���Һ�ֱ���5%NaHCO3����Һ��ˮϴ�����ԣ��پ������ᴿ�õ��������ױ���| ���� | n�������� | ���������и����칹������������%�� | �ܲ��� ��%�� | ||
| n���ױ��� | �������ױ� | �������ױ� | �������ױ� | ||
| ŨH2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 82.0 |
| 1.2 | 36.5 | 59.2 | 4.0 | 83.8 | |
NaHSO4 | 0.25 | 46.3 | 52.8 | 0.9 | 92.8 |
| 0.32 | 48.0 | 51.7 | 0.3 | 95.0 | |
| 0.36 | 45.0 | 54.4 | 0.6 | 93.9 | |
| �ܶ�/g•cm-3 | �е�/�� | �ܽ��� | |
| �ױ� | 0.866 | 110.6 | ������ˮ�������������ױ� |
| �������ױ� | 1.286 | 237.7 | ������ˮ��������Һ̬�� |
| �������ױ� | 1.162 | 222 | ������ˮ��������Һ̬�� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | δ��ȴ��ת�ơ����� | B�� | ����ƿ��ԭ����������ˮ | ||
| C�� | ����ʱ���ӿ̶��߹۲�Һ�� | D�� | ����ʱ�Ӷ���ˮ������������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com